Ион - одновалентная медь
Cтраница 1
Ион одновалентной меди, Си, не имеет незаполненной электронной оболочки и, следовательно, должен быть диамагнитным что как будто подтверждается [120, 121], хотя Перакис и Капатос [122] полагают, что он может быть слабо парамагнитным Если их предположение правильно, то это может быть тальке независимый от температуры парамагнетизм. При измерениях соединений закисной меди необходимо, конечно, исключить парамагнетизм двухвалентного иона меди. [1]
Ион одновалентной меди, взаимодействуя одновременно с нит-рильной группой и молекулой красителя, образует комплекс, хотя сам по себе кислотный краситель не обладает сродством к нитрильным группам. Существует ряд требований, выполнение которых необходимо для получения хороших результатов. [2]
Ион одновалентной меди и ион натрия имеют одинаковые размеры ( 0 98), однако, в силу резкой разницы в типах химической связи у соединений меди и натрия, изоморфные смеси натриевых и медных солей практически не встречаются. Соли натрия являются ионными соединениями, соли меди - ковалент-ными. Атом меди, кроме того, образует, как правило, небольшое число ( 3 - 4) ковалентных связей. Для нее справедливо все то, что сказано относительно структуры AgJ в § 4 главы XII о типах химической связи. [3]
Для крашения необходимы ионы одновалентной меди. Обычно в красильную ванну загружают сульфат окисной меди и восстанавливают ее in situ до одновалентной. [4]
Накопление в растворе ионов одновалентной меди в больших количествах приводит к сдвигу реакции влево, в результате чего выпадает металлическая губчатая медь. [5]
Неокупроин образует с ионами одновалентной меди комплексное соединение, окрашенное в желтый цвет. [6]
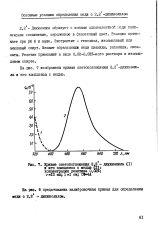 |
Кривые светопогдощения - и его комплекса с медью ( 2. концентрация реактива О, vIO мл. 1Г СФ4А. [7] |
Дяхинолил образует с ионами одновалентной меди комплексное соединение, окрашенное в фиолетовый цвет. Реакция протекает при рН 6 и выше. Экстрагент - гексанол, изоамиловый или амиловый спирт. Мешают определению меди цианиды, роданиды, окса-латы. Реактив применяют в виде 0 02 - 0 03 % - ного раствора в изоами-ловом спирте. [8]
Однако в растворе цианида ионы одновалентной меди удаляются в результате образования ионов комплексного цианида, и медный анод растворяется при этом как одновалентный элемент. Аноды из железа, свинца и олова растворяются почти всегда с образованием ионов низшей валентности. [9]
Таким образом, связывание ионов одновалентной меди в малораство-рймое соединение Cul приводит к резкому уменьшению концентрации [ Си ] и к увеличению окислительного потенциала системы Cu2 / Cu до величины Ех 0 76 в. Эта величина выше, чем величина окислительного потенциала иода ( при переходе в иодид), поэтому реакция между CuSO4 и KI протекает практически полностью слева направо. [10]
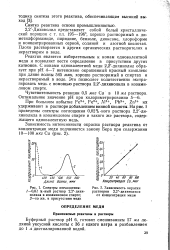 |
Спектры поглощения.| Зависимость окраски. [11] |
Реактив является избирательным к ионам одновалентной меди и позволяет вести определение в присутствии других катионов. С ионами одновалентной меди 2 2 -дихинолил образует при рН 4 - 7 интенсивно окрашенный красный комплекс при длине волны 545 ммк, хорошо растворимый в спиртах и нерастворимый в воде. Это позволяет количественно экстрагировать медь с помощью раствора 2 2 -дихинолила в изоами-ловом спирте. [12]
Бкцинхошшовая кислота взаимодействует с ионами одновалентной меди при рН 6 и выше. Гидролизующиеся ионы связываются винной кислотой и сульфитом натрия. [13]
Си до Си, то ионы одновалентной меди не могут существовать возле электрода в заметной концентрации. [14]
При анодном растворении могут образоваться ионы двухвалентной и одновалентной меди. [15]
Страницы: 1 2 3 4