Ион - двухвалентный металл
Cтраница 1
Ионы двухвалентного металла Ме2 и трехвалентного железа Fes в решетке ферритов MeO - Fe2O3 могут быть расположены по-разному, образуя при этом один из двух типов шпинели: прямую ( нормальную) или обращенную. [1]
 |
Схематическое изображение зависимости Ms - f ( T подрешеток А и В ала ферритов с точкой компенсации. [2] |
Ионы двухвалентного металла Ме2 и трехвалентного железа Ре в решетке ферритов MeO - Fe2O3 могут быть расположены по-разному, образуя при этом один из двух типов шпинели: прямую ( нормальную) или обращенную. [3]
Ионы двухвалентных металлов, в частности кальция, обеспечивают более действенную защиту полифосфатами. Поскольку кальций неизменно присутствует в естественных водах, то добавлять его обычно не приходится. Добавление солей кальция необходимо лишь в случае конденсата или мягких вод. Цинк более эффективен, чем кальций, хотя последний все же необходим. В более щелочных средах полифосфаты могут привести к точечной или питтинговой коррозии. [4]
Ионы двухвалентных металлов, например цинка, кальция, обеспечивают более действенную защиту полифосфатами. [5]
Ионы двухвалентного металла Ме2 и трехвалентного железа Fe3 в решетке ферритов MeO - Fe2O3 могут быть расположены по-разному, образуя при этом один из двух типов шпинели: прямую ( нормальную) или обращенную. [6]
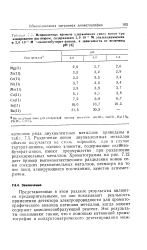 |
Исправленные времена удерживания ммм. ионов при элюировании раствором, содержащим 2 0 Ю 3 М этилендиаммония и 2 0 10 - 3 М т-оксиизобутират-аниона, в зависимости от величины. [7] |
Разделение ионов двухвалентных металлов обычно получается не столь хорошим, как в случае тартрат-аниона, однако элюенты, содержащие оксиизо-бутират-анион, имеют преимущество при разделении редкоземельных металлов. Хроматограмма на рис. 7.12 дает пример высококачественного разделения ионов семи соседних редкоземельных металлов, несмотря на то что пики, элюирующиеся последними, заметно асимметричны. [8]
В отсутствие ионов двухвалентных металлов гексаметафосфат может быть как ингибитором, так и стимулятором коррозии. Если скорость движения воды и содержание ингибитора малы, то гексаметафосфат входит в состав растворимого комплекса, что ускоряет анодную реакцию и соответственно коррозию. При увеличении содержания гексаметафосфата на поверхности металла осаждается пленка, замедляющая анодную реакцию и коррозию стали. [9]
Адсорбционная способность ионов двухвалентных металлов в интервале рН 5 - 8 колеблется между 0 2 и 0 5 моля М2 на 1 моль иминодипропионовой смолы. [10]
Для эффективного элюирования ионов двухвалентных металлов нужен такой катион, как этилендиаммо-ний. Поэтому катионы двухвалентных металлов превосходно элюируются в среде 2 0 - Ю-3 М тартрата этилендиаммония, но не в среде элюента, приготовленного из виннокислого натрия или аммония. [11]
Для изучения хроматографии ионов двухвалентных металлов на хелоновых смолах [92] ионы металлов подают в виде ацетатного буферного раствора ( рН 5 - 6) на колонку, заполненную монофункциональной иминодиуксусной смолой ( в избытке относительно ионов металлов) в нейтральной калиевой форме. При этом ионы металлов фиксируются на монофункциональной иминодиуксусной смоле в виде комплексов, а буфер нейтрализует освобождающиеся ионы водорода. [12]
Обычно дополнительную концентрацию ионов двухвалентного металла, например 7п2 - ионов, создают, вводя его окисел или гидроокись в заранее: подкисленный раствор. [13]
Соединения 8-оксихинолина с ионами двухвалентных металлов, имеющими обычно координационное число 6, если и экстрагируются из водного раствора хлороформом или подобными растворителями, то лишь неполностью, или дают с ними неустойчивые растворы, которые вскоре мутнеют. Речь идет о таких оксихинолинатах, которые образуют очень устойчивые дигидра-ты, труднорастворимые как в водной, так и в органической фазах. Мы попытались эту воду, принадлежащую, очевидно, к комплексной сфере [2], заменить полярными органическими соединениями и таким образом получить комплексы, растворимые в органических растворителях. Это удается при добавлении к водному раствору перед экстракцией приблизительно 2 % алифатического первичного или вторичного амина. [14]
Хотя прямые доказательства роли ионов двухвалентных металлов в металлзависимых окислительных декарбоксилазах в настоящее время отсутствуют, некоторые предварительные данные подтверждают, что ион металла участвует исключительно в образовании мостикового комплекса фермент - М2 - субстрат. [15]
Страницы: 1 2 3 4