Ион - двухвалентный металл
Cтраница 3
Очевидно, что захват коллоидной мицеллой гидроокиси ионов двухвалентных металлов, остающихся в растворе в виде комплексов, будет тем больше, чем больше ионов этих металлов, не связанных в комплекс, будет оставаться в растворе. [31]
Таким образом в сущности ряд селективности для ионов двухвалентных металлов на иминодипропионовой смоле совпадает с такими рядами для иминоуксуснопропионовой и иминодиуксусной смол. [32]
Очевидно, что захват коллоидной мицеллой гидроокиси ионов двухвалентных металлов, остающихся в растворе в виде комплексов, будет тем больше, чем больше ионов этих металлов, не связанных в комплекс, будет оставаться в растворе. [33]
Для большинства ферментов пока еще остается невыясненной роль ионов двухвалентных металлов. [34]
Херинг [102] в своей очередной работе ( Распределение ионов двухвалентных металлов между монофункциональной иминодиуксусной смолой и водным раствором низкомолекулярной нитрилотриуксус-ной кислоты при различных значениях рН) отмечает, что в слабокислом интервале рН наблюдаемые коэффициенты селективности можно вычислить из устойчивости комплексов нитрилотриуксусной кислоты и низкомолекулярной иминодиуксусной кислоты. [35]
После того как вытеснительная хроматография была разработана для ионов двухвалентных металлов, водной из работ [233] была предпринята попытка разделения ионов редкоземельных элементов разбавленными минеральными кислотами на монофункциональной иминодиуксуснои смоле. [36]
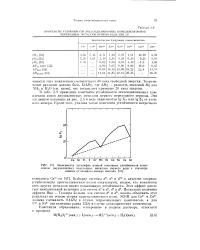 |
Зависимость логарифма полной копстанты устойчивости комплексов двухвалентных переходных металлов первого ряда с этиленди-амином от атомного номера металла. [37] |
В табл. 2.9 приведены константы устойчивости этилендиаминовых комплексов ионов двухвалентных металлов первого переходного периода. Эти же данные показаны на рис. 2.5 в виде зависимости lg KT или lg ( 33 т атомного номера. [38]
Ионы уранила были обсуждены в главе, посвященной ионам двухвалентных металлов, так как свойства UO22 1 с позиций комплексооб-разования приближаются к свойствам ионов двухвалентных металлов. [39]
Анион CioHi2OgN2H2 - - 2H2O, соединяясь с ионами двухвалентных металлов в щелочной среде, образует комплексные соединения триланатов. [40]
В качестве примера применения теории МО рассмотрим теплоту гидратации ионов двухвалентных металлов, показанную на рис. 2.7. Поскольку лигандом является вода, то я-связями можно пренебречь и считать орбитали tzg центрального атома несвязывающими. Таким образом, электроны, помещенные на эти орбитали, в грубом приближении МО не будут влиять на теплоту гидратации. [41]
Существенно, что при образовании хелатных комплексов анилов с ионами двухвалентных металлов ( исследовались комплексы с никелем и медью) проводимость резко падает, свидетельствуя о том, что электроны, вошедшие в связь азот - металл, не способны более участвовать в проводимости. Действительно, прочность связи азот - металл, характеризуемая стабильностью комплекса, для медного комплекса выше, чем для никелевого, и одновременно медный комплекс имеет более низкую проводимость. [42]
По-видимому, наиболее вероятным является предположение, что процесс входа ионов двухвалентных металлов в кристаллы типа хлористого натрия идет двумя стадиями. Первой стадией этого процесса, до определенной концентрации примеси, является образование твердого раствора замещения с ограниченной смешиваемостью. Это подтверждается нашими данными: при ничтожной концентрации микрокомпонента в растворе коэффициент кристаллизации является постоянным и не зависит от присутствия многовалентных ионов; подтверждается радиографическими исследованиями и данными увеличения проводимости кристалла при увеличении концентрации примесных двухвалентных ионов. Вторая стадия процесса, при концентрациях, больших предела смешиваемости - это образование адсорбционных систем, возможно адсорбция примеси на межкристаллических поверхностях. Чтобы проверить последнее предположение, нами было изучено влияние ионов висмута и алюминия на коэффициент кристаллизации в случае, когда содержание свинца выше той величины, которая отвечает образованию твердых растворов. [43]
Хорошо известно, что биологическая активность АТФ проявляется в присутствии ионов двухвалентных металлов, но точная природа взаимодействия между АТФ и этими ионами не была известна. Исследование ядерного магнитного резонанса протонов и релаксации 31Р в концентрированных растворах АТФ ( 0 35 моль / л) показало, что ионы Мп2 взаимодействуют с тремя фосфатными группами и частью аденино-вого кольца. По формулам ( 23) на основе экспериментальных значений времени релаксации были определены расстояния между ионами Мп2 и протонами кольца. [44]
Описаны многие нуклеотидил - и пентозилтрансферазы, которым необходима активация ионом двухвалентного металла [ обычно Мп2 и ( или) Mg2 ] [280], однако нет исследований, проливающих свет на роль иона металла в реакциях этого типа. [45]
Страницы: 1 2 3 4