Максимальный выход - продукт - реакция
Cтраница 2
Процентное содержание ( выход) йодистого водорода в равновесной смеси ( 71 2 %) получили меньше, чем в первом варианте ( 77 2 %), когда исходные вещества ( Н2 и 12) были смешаны в эквивалентных количествах. Можно доказать, что для любого типа реакций справедлив вывод: максимальный выход продукта реакции достигается тогда, когда исходные вещества смешаны в эквивалентных количествах. [16]
В случае, если целевой конечный продукт образуется при участии некоторого промежуточного вещества, высказанные соображения оказываются неверными. В этом случае существует некоторая оптимальная скорость подачи исходных веществ, обеспечивающая максимальный выход продукта реакции в единицу времени. Скорость образования продукта реакции определяется концентрацией промежуточного вещества. Но при слишком больших скоростях подачи последняя падает из-за быстрого вывода промежуточного вещества из системы. При слишком медленной подаче исходных веществ, как уже указывалось, падает концентрация исходных веществ, а следовательно, и скорость образования промежуточного вещества, что также приводит к уменьшению стационарной концентрации промежуточного вещества. [17]
В случае, если целевой конечный продукт образуется при участии некоторого промежуточного вещества, высказанные соображения оказываются неверными. В этом случае существует некоторая оптимальная скорость подачи исходных веществ, обеспечивающая максимальный выход продукта реакции в единицу времени. Скорость образования продукта реакции определяется концентрацией промежуточного вещества. Но при слишком больших скоростях подачи последняя падает из-за быстрого увода промежуточного вещества из системы. При слишком медленной подаче исходных веществ, как уже указывалось, падает концентрация исходных веществ, а следовательно, и скорость образования промежуточного вещества, что также приводит к уменьшению стационарной концентрации промежуточного вещества. [18]
Принцип Ле Шателье имеет большое практическое значение. На его основе можно подобрать такие условия осуществления химического взаимодействия, которые обеспечивают максимальный выход продуктов реакции. [19]
На его основе можно подобрать такие условия осуществления химического взаимодействия, которые обеспечивают максимальный выход продуктов реакции. [20]
Метод, в основе которого лежит термическое разложение образца с последующим анализом продуктов разложения каким-нибудь физическим или химическим способом, называют пиролизом. Образцы можно идентифицировать по температурам появления продуктов реакции; по числу образовавшихся продуктов; по температуре, при которой наблюдается максимальный выход продуктов реакции. [21]
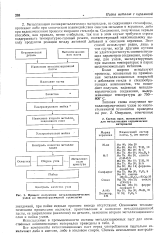 |
Процесс получения металлокерамических узлов по многоступенчатой технологии. [22] |
Металлизация поликрнсталлических материалов, не содержащих стсклофазы, протекает либо при химическом взаимодействии окислов металлов и керамики, либо при видоизмененном процессе миграции стеклофазы. Соединения, полученные первым способом, как правило, менее стабильны, так как в этом случае требуется строго поддерживать температурно-газовый режим, соответствующий максимальному выходу продуктов реакции между активной добавкой и окислами керамики. [23]
Говоря об оптимальном соотношении между реагентами, необходимо обратить внимание на следующее: если расход одного из них по тем или иным причинам лимитирован, то увеличение концентрации сореагентов позволит увеличить степень его использования; она будет тем большей, чем больше введено другого реагента. При этом надо иметь в виду не только затруднения, связанные с удалением из равновесной смеси избытка непрореагировавшего реагента, но и то обстоятельство, что для получения максимального выхода продуктов реакции нужна стехиометрическая смесь. [24]
 |
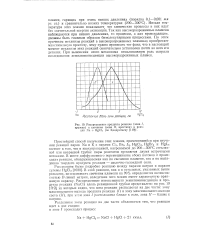
Зависимость выхода аммиака в peaкции V2N2 ( г 3 / 2Н2 ( г NH3 ( г от температуры и давления. [25] |
Говоря об оптимальном соотношении между реагентами, необходимо обратить внимание на следующее: если расход одного из них по тем или иным причинам лимитирован, то увеличение концентрации сореагентов позволит увеличить степень его использования; она будет тем большей, чем больше введено другого реагента. При этом надо иметь в виду не только затруднения, связанные с удалением из равновесной смеси избытка непрореагировавшего реагента, но и то обстоятельство, что для получения максимального выхода продуктов реакции нужна стехиоме-трическая смесь. [26]
 |
Распределение продукта реакции ( зона /, кружки и свечения ( зона / /, крестики в реакции Na HgCh ( по Кондратьеву. [27] |
В этой реакции, как и в остальных, указанных выше реакциях, интенсивность свечения пламени на 99 % определяется интенсивностью D-линий натрия, вследствие чего пламя имеет характерную оранжевую окраску. Распределение интенсивности хемилюминесценции и продукта реакции ( NaCl) вдоль реакционной трубки представлено на рис. 19 [119], из которых видно, что зона реакции распадается на две части: зону максимального выхода продукта реакции ( /) и зону максимального выхода света ( / /), при этом зона / расположена ближе к соли, зона / / - ближе к натрию. [28]
Наши работы показали, что при минимальных концентрациях наиболее активных катализаторов реакция окисления развивается с образованием в основном карбоновых кислот. С увеличением концентрации катализатора, при постоянной температуре наблюдается закономерное и постепенное снижение выхода карбоновых кислот и увеличение количества вторичных и третичных продуктов реакции - оксикислот и их эфиров. Вершина параболы соответствует максимальному выходу продуктов реакции ( карбоновых кислот или оксикислот и их эфиров) и оптимальной концентрации катализатора для данной температуры. [29]
Константы равновесия реакций определяют опытным путем или рассчитывают теоретически. Для некоторых сложных реакций константы равновесия можно вычислять по константам равновесия более простых реакции, из которых составляется сложная реакция. По константам равновесия рассчитывают состав равновесных смесей, максимальный выход продуктов реакции при заданных условиях, процент превращения исходных веществ в конечные продукты и другие важные показатели производственных процессов. [30]
Страницы: 1 2 3