Ион - никель
Cтраница 1
Ионы никеля элюируют водой, а затем серебро элюируют 7 % - ным раствором азотнокислого натрия. [1]
Ион никеля стремится притянуть к себе атом кислорода, тем самым высвобождая ион водорода. Другая причина состоит в том, что поверхностная вода приобретает кислотные свойства в результате индуктивного влияния соседних катионов, представляющих собой кислотные центры льюисовского типа. Таким образом, брен-стедовская кислотность появляется в том случае, когда при дегидратации у иона никеля образуется свободная орбиталь, причем с увеличением температуры прокаливания кислотность возрастает. Однако, поскольку с увеличением температуры прокаливания содержание гидратнои воды уменьшается, после достижения некоторой температуры бренстедовская кислотность начинает уменьшаться. Льюисовская кислотность также увеличивается с повышением температуры прокаливания, однако увеличение кислотности происходит лищь до тех пор, пока существует метастабильная структура, имеющая свободную орбиталь. Дальнейшее увеличение температуры вызывает распад метастабильной структуры и образование стабильной формы, что приводит к уменьшению льюисовской кислотности. Поэтому можно считать, что максимум бренстедовской кислотности наблюдается при более низкой температуре, а максимум льюисовской кислотности при более высокой и что сумма обеих кислотностей дает общую кислотность ( см. рис. 3 и 4), которую можно измерить экспериментально при титровании / ( - бутил-амином. [2]
Ионы никеля переходят в раствор, а элементарная сера остается на аноде, образуя пористую, хорошо проводящую ток, корку серного шлама. [3]
Ионы никеля не мешают этой реакции. [4]
 |
Микроструктура кобальтового покрытия (. к 15 А / дм . [5] |
Ионы никеля, меди, железа, марганца не мешают электролизу, a Cd 1 мг / л, As 3, Sb 10 и Hg 1 мг / л являются вредными примесями. Указанные примеси удаляют с помощью H2S при рН 4 путем кристаллизации и осаждения. [6]
Ион никеля образует два довольно устойчивых аммиачных комплекса. [7]
Ионы никеля в слабоаммиачной среде в присутствии сильного окислителя вступают в реакцию с диметилглиоксимом с образованием комплексного соединения красного цвета. Интенсивность окраски пропорциональна концентрации никеля. [8]
Ионы никеля в аммиачной среде с диметилглиоксимом образуют светло-красное нерастворимое в воде соединение, которое после отделения фильтрованием и высушивания при 110 - 120 С имеет постоянный состав. [9]
Ионы никеля в сла боаммиачной среде в присутствии сильного окислителя вступают в реакцию с диметилглиоксимом с обра-зованием комплексного соединения красного цвета. Интенсивность окраски пропорциональна концентрации никеля. [10]
Ионы никеля из раствора смеси катионов всех групп можно обнаружить, проявляя хроматограммы диметилглиоксимом. Первичную хроматограмму обрабатывают парами аммиака и каплей спиртового раствора диметилглиоксима; при этом образуется ярко-красная зона внутрикомплексной соли диметилглиоксимата никеля. [11]
Ион никеля образует два довольно устойчивых аммиачных комплекса. При добавлении большего количества раствора гидроокиси аммония осадок растворяется, давая голубой раствор, который при дальнейшем добавлении гидроокиси аммония становится светлым сине-фиолетовым. [12]
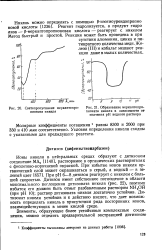 |
Светопропускание меркаптопро-пионата никеля.| Образование меркаптопро. [13] |
Ионы никеля в нейтральных средах образуют с дитизоном соединение МА2 [1140], растворимое в органических растворителях с фиолетово-коричневой окраской. При рН 6 - 8 дитизон реагирует с никелем с большой скоростью. Дитизон имеет собственное поглощение в области максимального поглощения дитизоната никеля ( рис. 22), поэтому избыток его должен быть отмыт разбавленным раствором NH4OH ( при рН 10); раствор дитизоната никеля достаточно устойчив. Ди-тизонат никеля устойчив и к действию кислот, что дает возможность определять никель в присутствии ряда посторонних ионов, взаимодействующих в менее кислой среде. [14]
Ионы никеля образуют с оксамидом [905] NH2COCONH2 в щелочной среде окрашенное в желтый цвет соединение. Интенсивность окраски увеличивается с прибавлением этанола или эфира. Реакции мешают катионы, образующие в щелочной среде окрашенные гидроокиси. [15]
Страницы: 1 2 3 4