Ион - ниобий
Cтраница 3
Мешают определению ниобия 10 - 50-кратные количества ионов V, W, Zr, Mo. Ионы тантала проявляют несколько меньшую каталитическую активность, чем ионы ниобия. [31]
Опыт показывает, что, изменяя рН раствора, очень часто можно провести последовательное осаждение и разделение различных катионов при помощи одного и того же органического осадителя. Так, например купферрон из сильнокислых растворов осаждает только ионы ниобия, тантала, титана, циркония, ванадия, железа ( III), олова и позволяет отделять их от неосаждающихся в тех же условиях ионов алюминия, хрома, урана ( VI), бериллия, марганца, никеля, кобальта, цинка, фосфора, бора. [32]
Опыт показывает, что, изменяя рН раствора, очень часто можно провести последовательное осаждение и разделение различных катионов при помощи одного и того же органического осадителя. Так, например, купферон из сильнокислых растворов осаждает только ионы ниобия, тантала, титана, циркония, ванадия, железа ( III), олова и дает возможность отделять их от неосаждающихся при тех же условиях ионов алюминия, хрома, урана ( VI), бериллия, марганца, никеля, кобальта, цинка, фосфора, бора. [33]
Опыт показывает, что изменяя рН раствора, очень часто можно провести последователнное осаждение и разделение различных катионов при помощи одного и того же органического осадителя. Так, например, купферон из сильнокислых растворов осаждает только ионы ниобия, тантала, титана, циркония, ванадия, железа ( III), олова и позволяет отделять их от неосаждающихся в тех же условиях ионов алюминия, хрома, урана ( VI), бериллия, марганца, никеля, кобальта, цинка, фосфора, бора. [34]
Ион Ш5 сравнительно легко меняет валентность на Nb4, что и сказывается на спектрах поглощения в видимой области. Как отмечалось выше, при низкотемпературной монодоменизации в масле происходит потеря кислорода кристаллами, что также вызывает восстановление ионов ниобия. [35]
Для разделения ионов ниобия и тантала в качестве сорбента используют измельченный уголь ДАУХ, насыщенный комплексообразую-щим реагентом - 8-оксихинолином. Разделение ионов ниобия и тантала основано на различии растворимостей их 8-оксихинолятов в виннокислых средах в присутствии минеральной кислоты. Ионы ниобия в этих условиях осаждаются при рН 3 6 - 6 5, ионы тантала - при рН 1 5 и ниже. [36]
Фторидный комплекс тантала экстрагируется бензолом из кислых растворов в присутствии метилового фиолетового51, родамина 6Ж52, бутилродамина Б52 и других органических соединений, способных в кислых растворах давать катионы. По величине оптической плотности окрашенных экстрактов находят количество тантала. Фотометрическому определению тантала не мешают небольшие количества ионов ниобия, а также титана, циркония и гафния. [37]
Поскольку вокруг этих ионов поле спонтанной поляризации будет частично компенсироваться собственным полем иона, то и условия переполяризации будут более легкими. Также возможно образование зародышей вблизи таких структурных ионов, которые замещают другие структурные ионы в решетке для кристаллов конгруэнтного состава. Например, для ниобата лития такими ионами являются ионы ниобия, замещающие ионы лития. [38]
Экстракционно-каталитический метод определения ниобия с применением БО и индикаторной реакции окисления о-аминофенола пероксидом водорода более избирателен, чем метод, основанный на проведении той же реакции в водной среде по отношению к ионам меди, никеля, титана, железа, хрома, кобальта и марганца. Определению ниобия не мешает 103 - 104-кратный избыток указанных ионов; мешают 10 - 50-кратные количества ионов ванадия, вольфрама, циркония и молибдена. Ионы тантала проявляют несколько меньшую каталитическую активность, чем ионы ниобия. Продолжительность определения ( без химической подготовки проб) составляет 20 - 30 мин. [39]
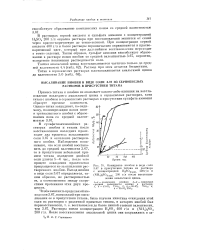 |
Осаждение ниобия в виде соли в присутствии титана из раствора. [40] |
В растворах серной кислоты и сульфата аммония с концентрацией H2S04 200 г / л окраска раствора при восстановлении меняется от синей через красно-коричневую до темно-зеленой. При концентрации серной кислоты 400 г / л и более растворы первоначально окрашиваются в красно-коричневый цвет, который при дальнейшем восстановлении переходит в темно-зелепый. Таким образом, сульфат аммония способствует образованию в растворе ионов ниобия со средней валентностью 3.67, вероятно, вследствие понижения растворимости соли. [41]
Наиболее полное использование ниобия достигается при восстановлении его алюминием. Этот метод широко применяют в промышленности. Максимально возможный уровень извлечения ниобия из Nb2Os при протекании алюминотер-мического восстановления по реакции 3Nb2O5 10Al 61 тЬ - - 5А12Оз определяется равновесными концентрациями ниобия в сплаве и оксида Nb2Os в шлаке. Высокотемпературное восстановление Nb2Os алюминием протекает в диффузионном режиме и лимитирующей стадией процесса является подвод ионов ниобия из оксидного расплава к границе раздела металлической и шлаковой фаз, поэтому повышение температуры расплава вызывает снижение концентрации Nb2O5 в шлаковом расплаве. [42]
Наиболее полное использование ниобия достигается npv восстановлении его алюминием. Этот метод широко применяют в промышленности. Максимально возможный уровеш извлечения ниобия из Nb2Os при протекании алюминотер-мического восстановления по реакции 3Nb2O5 10Al 61 тЬ 5А12Оз определяется равновесными концентрациями ниобия в сплаве и оксида Nb2Os в шлаке. Высокотемпературное восстановление Nb2O; алюминием протекает в диффузионном режиме и лимитирующей стадией процесса является подвод ионов ниобия из оксидного расплава к границе раздела металлической и шлаковой фаз, поэтому повышение температуры расплава вызывает снижение концентрации МЬ2Об в шлаковом расплаве. [43]
Давление кислорода изменялось в 50 раз - от 7 6 до 0 15 см. Простой зависимости между давлением и скоростью реакции не обнаружено. Подобные результаты получены и для окисления ниобия в том же самом интервале давлений. Очевидно, что линейное или пропорциональное квадратному корню из давления изменение скорости реакции не имеет места. Мы делаем вывод, что незначительное изменение скорости окисления при возрастании давления в 10 раз ( рис. 15) свидетельствует о том, что стадией, определяющей скорость этой реакции, является какой-то диффузионный процесс, возможно - диффузия ионов ниобия или тантала через окис-ную пленку. [44]
Электрическое поле может изменять не только оптические характеристики жидкостей и газов, оптически изотропных в отсутствие поля, но также и оптические свойства кристаллов. Это явление называется эффектом Поккелъса. Малая инерционность позволяет использовать эффект для высокочастотной модуляции света. В отличие от эффекта Керра, разность фаз волн Ех и Еу в кристалле оказывается пропорциональной первой степени напряженности поля. Изменение показателя преломления ( An) при эффекте Поккельса происходит за счет смещения электронов в сложном кристалле в сторону того или иного иона ( например, в случае ниобата лития LiNbOs - эт ион ниобия), при этом за счет изменения электронной конфигурации меняется поляризуемость, а с ней - и показатель преломления. В силу линейности эффект Поккельса может наблюдаться лишь в кристаллах, не обладающих центром симметрии. [45]
Страницы: 1 2 3