Равновесный выход - продукт
Cтраница 2
Равновесие реакции смещается при этом в правую сторону и равновесный выход продуктов увеличивается. [16]
Рассмотрим на нескольких примерах технологических гетерогенных процессов приемы увеличения равновесного выхода продукта. Эти приемы определяются количественной характеристикой равновесия рассматриваемых систем, основанной на законе распределения или правиле фаз. [17]
Однако при математическом моделировании процессов необходимо иметь непрерывную зависимость изменения равновесного выхода продукта от параметров процесса. Основными параметрами процесса пиролиза являются температура, давление и степень разбавления сырья. [18]
 |
Зависимость выхода продуктов от температуры процесса для экзотерических обратимых реакций ( т, Р, Ci, C2const. [19] |
Во-первых, для всех обратимых экзотермических процессов с повышением температуры снижается равновесный выход продукта и при некотором повышении температуры кинетика процесса вступает в противоречие с термодинамикой его; несмотря на повышение скорости прямого процесса, выход ограничивается равновесием. [20]
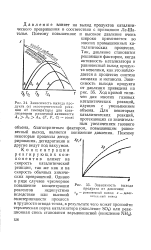 |
Зависимость выхода продукта ( х экзотермической реакции от температуры для катализаторов различной активности Ai AZ А3, ( Т, Р, Q const. [21] |
Так, давление становится решающим фактором, когда активность катализатора и равновесный выход продукта невелики, как это наблюдается в процессах синтеза аммиака и метанола. Ход кривой типичен для многих газовых каталитических реакций, идущих с уменьшением объема. [22]
Из данных, приведенных в табл. 10, видно, что равновесный выход продуктов реакций, в частности реакции полимеризации пропилена, при повышенных температурах очень незначителен. Это позволяет заключить, что практически для уменьшения содержания полимеров в алкилатах, а также с целью экономии сырья процесс алкилирования выгодно вести либо при температуре выше 250 С, либо при пониженной температуре и повышенных мольных соотношениях бензола и пропилена. [23]
Перечисленные выше положения позволяют установить диапазон условий, при которых возможен высокий равновесный выход продукта. Но для практического осуществления процесса знания этих условий недостаточно, так как необходимо не только получить большой выход продукта, но и обеспечить высокую скорость процесса, поскольку от нее в значительной степени зависит производительность аппаратуры. [24]
С; повышение температуры до 600 С увеличивает скорость реакции, но уменьшает равновесный выход продукта. [25]
 |
Константы равновесия реакций алкилирования изопро-пи л бензол а пропиленом в газовой фазе. [26] |
Полученные данные приведены в табл. 7, из которой видно, что с повышением температуры равновесный выход продуктов алкилирования снижается, а с повышением давления и мольного соотношения ароматического углеводорода и пропилена - возрастает. Следовательно, с термодинамической точки зрения производство моно - и диизопропилбензолов алкилиро-ванием бензола или изопропилбензола пропиленом целесообразно проводить при температурах не выше 600 - 650 и 550 - 600 К соответственно. [27]
Для процессов, сопровождаемых обратимой химической реакцией между твердыми и газообразными реагентами, равновесные концентрации и равновесный выход продукта определяются при помощи константы равновесия, рассчитанной по концентрациям или парциальным упругостям газообразных реагентов и газообразных продуктов реакции. При расчете константу равновесия выражают только через равновесные концентрации компонентов газовой фазы, поскольку значения упругости насыщенных паров твердых веществ малы и почти не изменяются. [28]
Для процессов, сопровождаемых обратимой химической реакцией между твердыми и газообразными реагентами, равновесные концентрации и равновесный выход продукта определяются при помощи константы равновесия, рассчитанной по концентрациям или парциальным давлением газообразных реагентов и газообразных продуктов реакции. При расчете константу равновесия выражают только через равновесные концентрации компонентов газовой фазы, поскольку парциальные давления насыщенных паров твердых веществ малы и почти не изменяются. Если реакция идет без изменения числа молей газа, равновесие зависит только от температуры. [29]
Так как процесс дегидрирования не только эндотермичен, но и сопровождается увеличением реакционного объема, то равновесный выход продуктов реакции растет с увеличением температуры и уменьшением парциальных давлений реагентов. [30]
Страницы: 1 2 3 4