Равновесный выход - продукт
Cтраница 3
Для обратимой эндотермической реакции, наоборот, снижение температуры приводит к смещению равновесия влево и уменьшению равновесного выхода продукта, а увеличение температуры - к сдвигу равновесия вправо. [31]
Знание числового значения константы химического равновесия позволяет рассчитать такие важные величины, как степень превращения исходных веществ, равновесный выход продуктов реакции, степень диссоциации исходного вещества. [32]
Для жидкофазной параллельной реакции, оба направления которой Ог 2Аз 5В имеют / Сс1, выявите условия, способствующие получению большего равновесного выхода продуктов. [33]
С другой стороны, значения / С, приведенные в таблицах, в ряде случаев вычислены по тем же формулам через равновесный выход продукта, который определили экспериментально. [34]
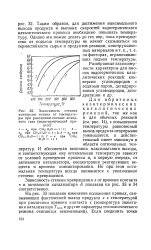 |
Зависимость степени конверсии метана от температуры при различном составе исходного газа ( эндотермический процесс. [35] |
Для обратимых экзотермических каталитических реакций, так же как и для обычных реакций ( см. рис. 14), с повышением температуры равновесный выход продукта непрерывно уменьшается, а действительный имеет максимум в области оптимальных температур. И абсолютная величина максимального выхода, и соответствующая ему оптимальная температура зависят от условий проведения процесса и, в первую очередь, от активности катализатора, концентрации реагирующих веществ и времени контактирования. Но при этом оптимальная температура всегда понижается с увеличением степени превращения. [36]
 |
Данные для расчета. [37] |
При положительном значении AF движущая сила связана, главным образом, с реакцией, идущей справа налево, но даже и в этом случае равновесный выход желательного продукта может быть существенным. [38]
Таким образом, определяемый уравнением ( 14) энергетический выход есть тог максимально возможный выход, который при заданных начальных параметрах процесса обусловлен лишь ходом равновесной кривой С л / о - FfTsJit достижим лишь при условии, что термодинамически равновесный выход продукта при температуре Tf полностью сохраняется при закалке. Это позволяет принять соответствующее значение в качестве энергетического критерия равновесности d в процессе плазмохимического окисления азота. [39]
Процесс дегидрирования проводят и при более высоких давлениях. Однако это снижает равновесный выход продуктов. Поэтому повышение давления требует применения более высоких температур. [40]
Равновесие в системе Ж - Т основано на правиле фаз и выражается при помощи диаграмм фазового состояния, определяющих зависимость состояния системы и фазовых равновесий в ней от ее состава или внешних условий. Анализ таких диаграмм позволяет определять равновесный выход продукта и условия максимального приближения реального производственного процесса к равновесию. [41]
Если после наступления равновесия в такой системе изменить температуру, например понизить ее, то, согласно принципу Ле-Ша - телье, в системе должны произойти изменения, компенсирующие снижение температуры и приводящие к ее повышению. Равновесие реакции смещается при этом в правую сторону и равновесный выход продуктов увеличивается. [42]
Скорости прямой и обратной реакции неодинаково зависят от перечисленных выше условий, поэтому соответствующим подбором температуры, давления и исходной концентрации реагентов можно увеличить равновесный выход. Например, если реакция протекает с поглощением тепла, то равновесный выход продукта при повышении температуры увеличивается. Среди обратимых реакций имеются такие, для которых достижение условий равновесия неблагоприятно сказывается на увеличении выхода продукта. [43]
С - число степеней свободы или вариантность системы; К - число независимых химических компонентов в системе; П - число внешних параметров, влияющих на равновесие фаз; Ф - число фаз) и выражается при помощи диаграмм фазового состояния, определяющих зависимость состояния системы и фазовых равновесий в ней от ее состава или внешних условий. Анализ таких диаграмм описан в литературе, он позволяет определить равновесный выход продукта и условия максимального приближения реального производственного процесса к равновесию. [44]
Если процесс протекает вблизи равновесия, то оптимальным должен быть стехиометрический состав смеси. Действительно, всякое отклонение исходного состава от стехиометрического будет вести к уменьшению равновесного выхода продуктов реакции, что видно из следующего. [45]
Страницы: 1 2 3 4