Ион - бикарбонат
Cтраница 2
Из уравнения видно, что в результате разложения двух ионов бикарбоната в высушенном остатке остается лишь один ион карбоната и величина сухого остатка оказывается меньше истинного значения. [16]
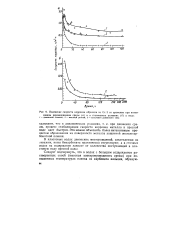 |
Изменение скорости коррозии образцов из Ст. 3 со временем при интен. [17] |
В пластовых водах девонских месторождений, извлекаемых из скважин, ионы бикарбоната практически отсутствуют, а в сточных водах их содержание зависит от количества поступающей в пластовую воду пресной воды. [18]
При нормальном значении рН крови ( 7 4) концентрация ионов бикарбоната НСО3 в плазме крови превышает концентрацию СО2 примерно в 20 раз. [19]
Растворы модифицированной соды и сесквикарбоната натрия менее щелочные, так как ион бикарбоната НСО3 в присутствии соды действует как кислота и смещает реакцию образования гидрок-сильных ионов влево. [20]
Наличие солей жесткости и ионов карбоната, образующихся в результате гидролиза ионов бикарбоната при нагревании артезианской воды, подобно поверхностным водам приводит к образованию осадка при их применении на промышленных предприятиях. Высокое содержание кремниевой кислоты также может привести к появлению в котлах твердой накипи, тогда как углекислота, образующаяся в результате смещения бикарбонатно-го равновесия системы, способствует образованию кислого конденсата. [21]
Наличие солей жесткости и ионов карбоната, образующихся в результате гидролиза ионов бикарбоната при нагревании артезианской воды, подобно поверхностным водам приводит к образованию осадка при их применении на промышленных предприятиях. Высокое содержание кремниевой кислоты также может привести к появлению твердой накипи, тогда как углекислота, образующаяся в результате смещения бикарбонатного равновесия системы, способствует образованию кислого конденсата. [22]
Начальная стадия может заключаться в реакции амина с двуокисью углерода или ионом бикарбоната с потерей протона. [23]
При нагреве и испарении морской воды парциальное давление СО2 в воде уменьшается; ионы бикарбонатов распадаются на ионы карбонатов, воду и газ С02, выделяющийся из воды при кипении. [24]
Вследствие малой диссоциации иона бикарбоната можно считать, что все ионы карбоната превратятся в ионы бикарбоната. [25]
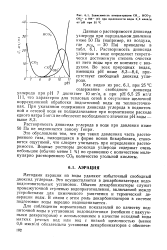 |
Зависимость концентрации СО. HCO-i СО2 - и ОН - ( С при щелочности воды 0 8 мэкв / л от рН при 25 С. [26] |
Это обусловлено тем, что при таких давлениях часть растворенного газа, находящаяся в форме ионов бикарбоната, становится ощутимой, что следует учитывать при определении растворимости. Водные растворы диоксида углерода содержат очень небольшое ( обычно менее 1 %) по сравнению с количеством моле-кулярно растворенного СО2 количество угольной кислоты. [27]
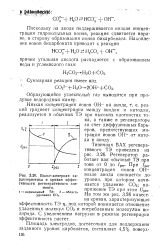 |
Вольт-амперная характеристика и кривая эффективности регенеративного элемента. [28] |
Поскольку на аноде поддерживается низкая концентрация гидроксильных ионов, реакция сдвигается вправо, в сторону образования ионов бикарбоната. [29]
Если в крови увеличивается количество оснований, то они, взаимодействуя со слабой угольной кислотой, образуют ионы бикарбоната и воду. [30]
Страницы: 1 2 3 4