Ион - бикарбонат
Cтраница 3
Остерлинд [113,119] пошел даже дальше, чем Стиман-Нильсен и Руттнер, утверждая, что некоторые растения используют ионы бикарбоната более эффективно, чем молекулы двуокиси углерода. По мнению Остер-линда, это увеличение не является результатом повышения щелочности, а вызывается присутствием ионов бикарбоната. Максимальная скорость роста была достигнута, когда [ НСО ] превосходила 9 10 - 6 моль. НСО П - Остерлинд полагал, что у примененной клеточной популяции не может наступить истощения двуокиси углерода даже в растворах, не содержащих бикарбонатных ионов. Он заметил также, что в присутствии 10 10 - 6 моль / л HCOjf рост идет в 25 раз быстрее, чем в присутствии 10 10 - 6 моль / л двуокиси углерода; отсюда он сделал вывод, что Scenedesmus quadricauda использует бикарбонатные ионы ( для роста и потому, повидимому, также для фотосинтеза) в 25 раз эффективнее, чем свободные молекулы двуокиси углерода. Позднее Остерлинд [121] нашел, что Chlorella pyrenoidosa не использует бикарбонатов. Не обнаружив никакого различия в содержании карбоангидразы у обоих видов, он предположил, что различны их клеточные оболочки. [31]
Известно, что пресные воды рек, применяемые для закачки в пласт на месторождениях Урало-Поволжья, характеризуется значительным содержанием ионов бикарбоната и кальция. [32]
Таким образом, вытеснение углекислоты из бикарбонатов плазмы в момент насыщения крови в легочных капиллярах кислородом происходит в результате проникновения части ионов бикарбонатов плазмы в эритроциты. Точно так же в тканевых капиллярах образование бикарбонатов фактически происходит в эритроцитах ( НаСОа К-НЬ - - КНСО3 Н - Hb), но затем часть ионов НСО3 - выходит из клеток в плазму, а на их место из плазмы в эритроциты поступают ионы хлора. [33]
При выборе типа реагента - извести, гипса или хлорида кальция - следует учитывать, что известь повышает рН раствора за счет ионов ОН - и переводит ионы бикарбоната в карбонатные. При использовании гипса и СаС12 гидроксильные ионы не образуются. Точность расчета снижается также еще и потому, что используемые известь, гипс, СаСЬ не являются химически чистыми реагентами и не соответствуют стопроцентной их активности. Считают, что для поддержания технологических свойств бурового раствора в него следует вводить этих добавок в 3 - 4 раза больше, чем получено из расчета: извести 0 123 кг и гипса 0 289 кг на 1 м3 раствора. [34]
Даже пси использовании для концентрирования морской воды ионообменных мембран, селективных по отношению к одновалентным ионам, некоторое количество ионов кальция проникает через катионообменную мембрану, а ионов бикарбоната - через анионооб-менную мембрану. При сильной поляризации через анионообменную мембрану проникают также ионы гидроксила, образующиеся в результате диссоциации воды, которые повышают рН раствора в камере концентрирования. При высоких значениях рН карбонат кальция осаждается и закупоривает камеры концентрирования. Если все же образуются осадки в камерах концентрирования, исходная питательная морская вода подкисляется, чтобы ионы водорода переносились через катионообменные мембраны и подкисляли раствор в камерах концентрирования. При подкислении раствора нерастворимые карбонаты переводятся в растворимые. [35]
При экономическом сравнении реагентного умягчения и ионного обмена следует иметь в виду, что при известково-содовом процессе расходуемое количество извести и карбоната натрия зависит от содержания в исходной воде ионов бикарбоната, кальция и магния, а также от соотношения между ними, тогда как при Na-катионировании количество соли, необходимой для регенерации, зависит только от общей жесткости воды. [36]
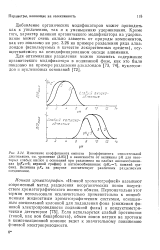
Шутова [38] и Руттнера [111,114], которые были истолкованы Рутт-нером ] Н4 ] и Остерлиндом [113,119] в том смысле, что некоторые водяные явнобрачные растения и водоросли могут весьма эффективно использовать ионы бикарбоната и поэтому наличие минимальных концентраций свободных молекул СО2 не является необходимым для поддержания их фотосинтеза. С другой стороны, водяные мхи вроде Fontinalis прекращают выделять О2, когда [ СО2 ] уменьшается примерно до значения 0 4 - 10 - 5 моль. Это соответствует 0 01 об. % С02 в атмосфере и означает, что компенсационный пункт у этих мхов имеет примерно то же значение, что и у наземных растений. [37]
Более ранние наблюдения Шутова [38], Боде [ 40J и Дама [ 39J, обнаруживших, что многие водяные растения могут повышать рН среды до таких значений, как 11 8 ( Spirogyra), можно тогда истолковать в том смысле, что эти растения могут использовать ионы бикарбоната непосредственно как источник углерода для фотосинтеза или, точнее, как средство для переноса двуокиси углерода из среды в клетки. [38]
Поскольку именно ион арсенита, а не мышьяковистая кислота, является катализатором интересующей нас реакции, то надо установить, остается ли арсенит полностью ионизированным в массе жидкости у низа колонны, а также не подавляется ли ионизация арсенита в диффузионной пленке из-за более высокой по сравнению с массой жидкости концентрации иона бикарбоната. [39]
NH Cl ослабляет влияние силикатов при определении кальция, но почти не устраняет влияния со стороны фосфатов и алюминия; 2) влияние со стороны фосфатов, алюминия и силикатов при определении магния значительно меньше, чем при определении кальция; 3) присутствие кальция при определении магния значительно ослабляет влияние силикатов и несколько уменьшает степень влияния фосфатов; 4) малые концентрации сульфатов и бикарбонатов ( до 400 мкг / мл иона бикарбоната) не оказывают влияния при определении кальция от 8 до 40 мкг / мл и магния от 4 до 20 мкг / мл, но влияние сульфатов имеется. [40]
Важнейшими анионами природных вод являются бикарбонат - и карбонат-ионы, а также хлор-ион и сульфат-ион. Ионы бикарбоната, карбоната и сульфата генетически связаны с ионами натрия и калия. Известный химик и гидрогеолог М. Г. Ва-ляшко связывает порядок чередования анионов и катионов при минерализации природных вод с растворимостью образуемых ионами солей. [41]
В пластовых водах содержание ионов бикарбоната слишком мало, чтобы оказать заметное влияние на кинетику коррозионного процесса. Дополнительное поступление в пластовые воды ионов бикарбоната и кислорода с пресными водами в процессе подготовки нефти частично создает условия для образования на металле защитных пленок. [42]
Для отрицательно заряженного комплекса СОз возможны две структуры. Первая по аналогии с ионами бикарбоната или карбоната имеет плоскую форму с атомом углерода, расположенным в центре треугольника из кислородных атомов. [43]
Для отрицательно заряженного комплекса СО3 возможны две структуры. Первая по аналогии с ионами бикарбоната или карбоната имеет плоскую форму с атомом углерода, расположенным в центре треугольника из кислородных атомов. [44]
Страницы: 1 2 3 4