Ион - бромоний
Cтраница 2
Работы Ола, несомненно, проливают новый свет на первоначально неизвестные детали реакций ароматического замещения с очень сильными электрофильными агентами, такими, как соли иона нитрония, образующиеся в ходе реакции ионы бромония или карбония, реакции которых представляют собой стадию, поддающуюся кинетическому контролю. [16]
Электрофальнзя атака бромом сопряженной диеновой системы дает интермедиат типа аллильного катиона. Стабильность аллильной системы, по-видимому, уменьшает необходимость образования прочного иона бромония. [17]
Электрофальная атака бромом сопряженной диеновой системы дает интермедиат типа аллильного катиона. Стабильность алллльной системы, по-видимому, уменьшает необходимость образования прочного иона бромония. [18]
Электрофальнзя атака бромом сопряженной диеновой системы дает интермедиат типа аллильного катиона. Стабильность аллильной системы, по-видимому, уменьшает необходимость образования прочного иона бромония. [19]
Атака С1 [15], 1 [16] и RS [17] аналогична атаке Вг, и здесь тоже может реализоваться множество механизмов, включающих в качестве крайних случаев образование циклических интермедиатов и катионов с открытой цепью. Как и следует ожидать, иодониевые ионы конкурируют с открытыми карбо-катионами более эффективно, чем ионы бромония, тогда как для ионов хлорония эта конкуренция менее эффективна. [20]
Пространственные условия нуклеофильной атаки л-комплекса и иона карбония, в котором осуществляется свободное вращение вокруг бывшей двойной связи, не одинаковы. В я-комплексе они напоминают условия подхода нуклеофила в реакциях типа 8ы2, поэтому присоединение нуклеофила к иону бромония происходит с противоположной стороны относительно связи между бромом и углеродом. Такая стереоспе-цифичность называется ягранс-присоединением. [21]
Ион бромония может быть атакован любым присутствующим в системе нуклеофилом, а не только ионом Вг6, что объясняет образование смешанных продуктов. Еще более важно, что этот механизм объясняет и стереохимию, так как замещение у атома углерода в ионе бромония должно протекать с обращением конфигурации, приводя в конечном счете к транс-присоединению, и так как олефины цис - и транс-строения должны образовывать различные ионы бромония. [22]
Только аксиальный заместитель при р-углеродном атоме способен играть роль соседней группы в реакциях замещения соединений циклогексана ( ср. Примеры этого были недавно изучены Альтом и Бартоном ( Alt, Barton, 1954); 2 ( 3 - ( а) - бромхолестанол - За ( а) - ( ЬХХУ) при действии бромисто-водородной и уксусной кислот дает 2р ( а), За ( а) - дибромхолестан с промежуточным образованием иона бромония ( ср. Соответствующее диэква-ториальное соединение ( 2а - бромхолестанол - 3р -) нереакционно-способно. [23]
Из данных табл. 5.5 следует обратить внимание на то, что скорости хлорирования и бромирования ъщс - и трянс-бутенов-2, с одной стороны, и изобутилена - с другой, мало отличаются между собой. Это является еще одним аргументом в пользу образования бромонневого иона. Благодаря циклической структуре ион бромония стабилизируется почти в одинаковой степени, независимо от того, находятся ли две метильные группы у одного ( в изобутилене) или у разных ( в бутенах-2) атомов углерода. Открытый карбокатион значительно более стабилен, если обе метильные группы связаны с карбокатиоиным центром. [24]
Главным постулатом этой теории является то, что атом углерода вывернут наизнанку в момент присоединения иона брома. С помощью таких теоретических представлений удовлетворительно объясняются реакции вытеснения. Как мы увидим в дальнейшем, ионы бромония, образовавшиеся из несимметричных олефинов, реагируют, давая более устойчивые ионы карбония. Если присоединять бром к олефину в растворе спирта, то ион бромония может атаковать спирт, образуя простые эфиры. [25]
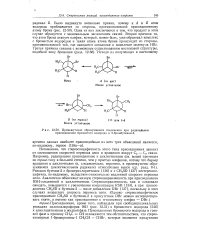 |
Промежуточно образующиеся соединения при радикальном присоединении бромистого водорода к 2-бромбутенам - 2. [26] |
Одна из них заключается в том, что продукт в этом случае образуется с минимальным заслонением связей. Вторая причина та, что атом брома атакует олефин, который, может быть, уже образовал комплекс с бромистым водородом и такая атака атома брома происходит со стороны, противоположной той, где находится связанная в комплексе молекула НВг. Третья причина связана с возможным существованием мостиковой структуры, подобной иону бромония ( разд. [27]
Главным постулатом этой теории является то, что атом углерода вывернут наизнанку в момент присоединения иона брома. С помощью таких теоретических представлений удовлетворительно объясняются реакции вытеснения. Как мы увидим в дальнейшем, ионы бромония, образовавшиеся из несимметричных олефинов, реагируют, давая более устойчивые ионы карбония. Если присоединять бром к олефину в растворе спирта, то ион бромония может атаковать спирт, образуя простые эфиры. [28]
Кроме того, должны существовать определенные препятствия для вращения вокруг связи а - Ь, так как иначе пгрео-и э / шт / ю-формы легко переходили бы друг в друга. Незначительный переход наблюдается, но он затрагивает лишь около 5 % продукта ацетолиза и еще меньшую долю продукта формолиза. Такие ионы Крам называет ионами фенония. Ион ( 21) имеет плоскость симметрии, и инвертирующая реакция с растворителем может приводить только к рацемическому продукту трео-конфи-гурации. Инвертирующая реакция иона ( 23) может протекать по атомам углерода а или b и приводит к одному и тому же э / штро-продукту ( 24) с сохраненной конфигурацией. Поэтому гипотеза фено-ниевых ионов не столь изящна, как теория ионов бромония, убедительно объяснившая явления, которые казались совершенно не связанными. [29]
Страницы: 1 2