Ион - переменная валентность
Cтраница 2
 |
Влияние некоторых оксидов на электропроводность стекол. [16] |
При наличии в стекле ионов переменной валентности ( V, РЬ, Fe) может иметь место и электронная проводимость, тогда стекла становятся полупроводниками. Полупроводниковыми являются халькогенидные стекла. Увеличение в составе стекла концентрации оксидов щелочных металлов приводит к уменьшению р, причем действие ионов малого радиуса более сильно, чем ионов большого радиуса. [17]
При введении в стекло ионов переменной валентности возникает конкуренция между ними и структурными центрами захвата. [18]
Переходы слабосвязанных электронов между ионами переменной валентности, и в частности от одного иона железа к другому, являются причиной электропроводности ферритов. Чем больше ионов Fe2 в ферритах, тем больше их удельная электрическая проводимость, величина которой может колебаться от 2 - Ю2 до 10 - ц ом-1. При повышении температуры спекания увеличивается концентрация ионов Fe2, а следовательно, и электропроводность ферритов. [19]
Как известно, каталитическое действие ионов переменной валентности может быть обусловлено или а) переходом электрона от иона к субстрату с возникновением свободного радикала, продолжающего реакцию, или б) взаимодействием катиона с молекулой электроно-донорного реагента. В случае ( б) катион переменной валентности, притягивая электронную пару, выступает л качестве катализатора, активирующего молекулу субстрата, подобно протону и кислотном катализе. Чалтыкяна приводят к выводу, что процессы ( а) и ( б) представляют собой крайние проявления катализа. Во многих случаях молекула одного и того же вещества в зависимости от состава раствора ( свойств среды) и физических условий находится в различных структурных состояниях и проявляет в одних условиях в большей степени электронодонорные, а в других электроноакцепторные свойства. Благодаря этому параллельно протекают как процесс ( а), так и процесс ( б), но с различными статистическими весами. [20]
Как известно, каталитическое действие ионов переменной валентности может быть обусловлено или а) переходом электрона от иона к субстрату с возникновением свободного радикала, продолжающего реакцию, или б) взаимодействием катиона с молекулой электроно-донорного реагента. В случае ( б) катион переменной валентности, притягивая электронную пару, выступает в качестве катализатора, активирующего молекулу субстрата, подобно протону в кислотном катализе. Чалтыкяна приводят к выводу, что процессы ( а) и ( б) представляют собой крайние проявления катализа. Во многих случаях молекула одного и того же вещества в зависимости от состава раствора ( свойств среды) и физических условий находится в различных структурных состояниях и проявляет в одних условиях в большей степени электронодонорные, а в других электроноакцепторные свойства. Благодаря этому параллельно протекают как процесс ( а), так и процесс ( б), но с различными статистическими весами. [21]
Интересна попытка сопряжения реакции фотоокисления воды ионами переменной валентности [60] с реакцией на полупроводниках, Красновским и Брин [60] установлено, что освещение близким УФ-излучением суспензий ZnO в водном растворе КзРе ( СМ) е сопровождается восстановлением ионов Fe ( CN) g и выделением молекулярного кислорода. [22]
Тушение того или иного вида вызывают обычно ионы переменной валентности - окислители и восстановители; ионы металлов переходной группы, в особенности железо, кобальт, никель; многие органические вещества, иногда - высокое содержание в растворе инертных солей; ионы брома, йода, серебра, окислы азота, в некоторых растворах - кислород воздуха. Часто удается путем маскировки соответствующими ком-плексообразователями устранить химические причины влияния посторонних веществ; действие физических причин обычно резко снижается при достаточном разбавлении растворов. [23]
Если в реакции продолжения цепи принимают участие ионы переменной валентности, то в кинетическое уравнение помимо концентраций исходных веществ входит концентрация ионов. [24]
Аналогичный механизм лежит в основе каталитического действия ионов переменной валентности, например, меди, железа, кобальта и др., при окислении таких субстратов, как аскорбиновая кислота, цистеин, тиогликолевая кислота. В некоторых случаях удалось выделить соответствующие промежуточные продукты, образуемые металлом в низшей степени окисления. Так, по Михаэлису и Шуберту, в отсутствие воздуха тиоглкколевая кислота образует с кобальтом хелат бледно-зеленого цвета, содержащий две молекулы кислоты на один ион двухвалентного кобальта. [25]
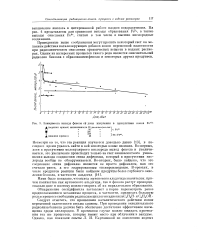 |
Зависимость выхода фенола от дозы излучения в присутствии ионов Fe 2. i ( верхняя кривая интенсивность 23 рентген1мл. сек ]. [26] |
Следует отметить, что проявления каталитического действия ионов переменной валентности весьма сложны. При проведении окислительного радиолиза бензола должно быть обеспечено достаточно эффективное насыщение среды кислородом. В противном случае можно ожидать протекания тех же процессов, которые имеют место при облучении в вакууме. [27]
Они находят применение в качеСтйе восстановителей или окислителей ионов переменной валентности. [28]
Как мы видели выше, в растворах, содержащих ионы переменной валентности, могут создаваться свободные радикалы, инициирующие радикальные реакции в растворенном веществе. [29]
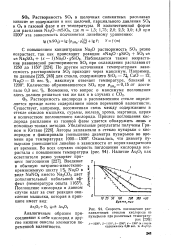 |
Скорость поглощения расплавленным стеклом кислорода из пузырьков при различных температурах. [30] |
Страницы: 1 2 3 4