Ион - низшая валентность
Cтраница 2
Однако в процессе эксплуатации происходит постепенное восстановление ионов V5 в ионы низшей валентности, которые не обладают ингибирующим действием. [16]
Высокие температуры способствуют так называемому бестоковому переносу металла вследствие реакций диспропорционирования ионов низшей валентности. Этим путем металлические электроды могут загрязняться более электроотрицательными металлами, вследствие чего их потенциалы становятся иными. [17]
Специфическая особенность расплавленных солей заключается в том, что в них могут существовать ионы низших валентностей наряду с обычными. [18]
Такой повышенный выход по току иногда может служить косвенным доказательством образования на аноде ионов низшей валентности. При этом должна учитываться возможная коррозия анодного металла. Если с учетом коррозии анодный выход по току превышает 100 %, можно сделать предположение относительно образования ионов различной валентности. [19]
На катоде могут протекать одновременно несколько сопряженных процессов: восстановление ионов шестивалентного хрома до ионов низшей валентности и до металлического хрома и восстановление ионов водорода. Хотя механизм восстановления ионов хрома явился предметом многих исследований [1,2], чрезвычайная сложность явлений, сопровождающих процесс хромирования, не позволяет пока считать решение этого вопроса окончательным. [20]
В некоторых случаях применяют аноды из растворимого и нерастворимого металлов, когда растворение происходит с образованием нежелательных ионов низшей валентности, например при осаждении высокооловянистой бронзы ( олово в качестве анода не применяется), или из одного нерастворимого металла, когда применение растворимых анодов неэкономично. [21]
Концентрации с т и с п могут быть определены, если учесть реакцию ( 2) взаимодействия ионов низшей валентности со сплавом при установлении равновесия. [22]
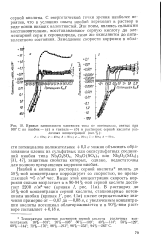 |
Кривые зависимости плотности тока от потенциала, снятые при 100 С на ниобии - ( а и тантале - ( б в растворах серной кислоты различных концентраций ( вес. %. [23] |
С энергетической точки зрения наиболее вероятно, что в условиях опыта ниобий переходит в раствор в виде ионов низших валентностей. Эти ионы, являясь сильными восстановителями, восстанавливают серную кислоту до элементарной серы и сероводорода, сами же окисляются до пятивалентного состояния. [24]
Совершенно аналогично можно решить задачу об обострении и размывании границы зон ионов при вытеснении ионов высшей валентности ионами низшей валентности. [25]
При пропускании через раствор постоянного электрического тока катионы электролита под влиянием электронов источника тока восстанавливаются на катоде в ионы низшей валентности, нейтральные атомы или атомные группы. Продукты восстановления отлагаются на катоде, вступают в реакции с молекулами растворенных веществ или растворителя или, наконец, реагируют с материалом электрода. В то же время анионы окисляются на аноде. [26]
При пропускании через раствор постоянного электрического тока катионы электролита под влиянием электронов источника тока восстанавливаются на катоде в ионы низшей валентности, нейтральные атомы или атомные группы. Продукты восстановления отлагаются на катоде, всту пают в реакции с молекулами растворенных веществ или растворителя или, наконец, реагируют с материалом электрода. В то же время анионы окисляются на аноде. [27]
При пропускании через раствор постоянного электрического тока ионы электролита, соприкасаясь с катодом, под влиянием электронов источника тока восстанавливаются в ионы низшей валентности, нейтральные атомы или атомные группы. Продукты восстановления отлагаются на катоде, вступают в реакции с молекулами растворенных веществ или растворител или, наконец, реагируют с материалом электрода. В то же аре-мя ионы, соприкасаясь с анодом, окисляются. [28]
Всякая расплавленная соль по отношению к любому металлу является агрессивной средой, потому что она содержит катионы, способные восстанавливаться до - ионов низших валентностей, элементарного состояния или сплавов с корродирующим металлом. В явном виде этот процесс наблюдается в среде расплавленных галогенидов щелочных металлов, у которых анионы не участвуют в процессе окисления. [29]
Вследствие восстанавливающей способности сероводорода при осаждении им катионов IV и V аналитических групп наблюдается превращение ионов различных окислителей, присутствующих в растворе, в ионы низшей валентности. Если окисление сероводорода при этом идет до элементарной серы, то она осаждается вместе с сульфидами катионов IV и V аналитических групп. [30]
Страницы: 1 2 3 4