Вычисление - коэффициент - активность
Cтраница 1
Вычисление коэффициентов активности по приведенным формулам для ( д 1 0 не практикуется, так как фактические индивидуальные значения этих коэффициентов для различных ионов, несмотря на их равновалентность, могут весьма сильно отличаться друг от друга, в то время как вычисленные по формуле они получились бы одинаковыми. [1]
 |
Модель ионной атмос-феры по Дебаю и Гюккелю где V2 - оператор Лапласа. [2] |
Вычисление коэффициентов активности по Дебаю и Гюккелю сводится к нахождению выражения энергии Лцг через свойства растворов, доступные прямому определению. [3]
 |
Модель ионной атмос-феры по Дебаю и Гюккелю где V -оператор Лапласа. [4] |
Вычисление коэффициентов активности по Дебаю и Гюккелю сводится к нахождению выражения энергии Д л / через свойства растворов, доступные прямому определению. [5]
Вычисление коэффициентов активности из уравнений ( 44) и ( 48) является в значительной степени аналитическим, потому что члены, содержащие оср и dX, весьма мало влияют на окончательный результат. Скэтчард [30] предложил формальный, чисто аналитический метод вычисления коэффициента активности и осмотического коэффициента, однако обычно пользуются графическим способом. [6]
Вычисление коэффициентов активности для компонентов в неидеальной реакционной смеси - сложная проблема, в настоящее время еще не решенная. Поэтому ниже рассматриваются системы, которые образуют идеальные растворы. Предположение о том, что раствор ведет себя как идеальный, справедливо для большинства газообразных систем. [7]
Вычисление коэффициентов активности из уравнений ( 44) и ( 48) является в значительной степени аналитическим, потому что члены, содержащие 8ср и dX, весьма мало влияют на окончательный результат. Скэтчард [30] предложил формальный, чисто аналитический метод вычисления коэффициента активности и осмотического коэффициента, однако обычно пользуются графическим способом. [8]
Вычисление коэффициентов активности отдельных ионов можно было бы произвести по коэффициенту активности соли, если известен коэффициент активности второго иона. Тогда, предполагая, что коэффициент активности отдельного иона зависит лишь от ионной силы раствора, можно, переходя от одного электролита к другому ( с общим ионом), вычислить коэффициенты активности отдельных ионов. Такой расчет, в силу некоторой произвольности исходных данных и невозможности распространения правила ионной силы на любые концентрации, не может дать точных результатов, хотя для практических целей весьма удобно считать коэффициенты активности ионов одинаковой валентности приблизительно равнцми, если одинаковы ионные силы растворов. [9]
Вычисление коэффициентов активности отдельных ионов можно было бы произвести по коэффициенту активности соли, если известен коэффициент активности второго иона. Тогда, предполагая, что коэффициент активности отдельного иона зависит лишь от ионной силы раствора, можно, переходя от одного электролита к другому ( с общим ионом), вычислить коэффициенты активности отдельных ионов. [10]
Однако вычисление коэффициента активности можно рассчитать более точно по понижению температуры замерзания. [11]
Метод вычисления коэффициента активности по экспериментальным данным [ см. уравнение (8.7) ] позволяет определить лишь значения средних коэффициентов активности электролита. В настоящее время не существует методов экспериментального определения коэффициентов активности отдельных ионов. При необходимости расчета этих величин обычно принимают, что средний коэффициент активности электролита представляет собой среднее геометрическое коэффициентов активности образующих его ионов. [12]
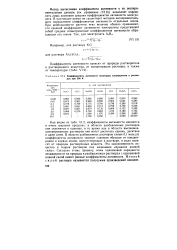 |
Коэффициенты активности некоторых электролитов в растворах при 298 К. [13] |
Метод вычисления коэффициента активности Y по экспериментальным данным [ см. уравнение (VI.8) ] позволяет определить лишь значения средних коэффициентов активности электролита. В настоящее время не существует методов экспериментального определения коэффициентов активности отдельных ионов. При необходимости расчета этих величин обычно принимают, что средний коэффициент активности электролита представляет собой среднее геометрическое коэффициентов активности образующих его ионов. [14]
Страницы: 1 2 3 4