Ион - рений
Cтраница 1
Ионы рения ( VII) можно определять полярографически ( см. стр. [1]
 |
Спектр светоиогло - конц. НС1 Re ( VII находится в виде щения перрепат-иона в иоде HRe03Cl, а в концентрированных. [2] |
Поведение ионов рения в водных растворах очень сложно вследствие его склонности к гидролизу и диспропорционированию и многообразия образующихся ионных форм. Наиболее устойчивыми являются соединения рения ( УП), комплексные галогенидные соединения рения ( У) и рения ( 1У), а также комплексные соединения рения ( У) и рения ( 1У) с различными органическими и неорганическими лигандами. Поэтому многие методы определения и выделения рения, которые в большинстве своем связаны с проведением реакций в водных растворах, основаны на использовании свойств именно этих соединений. [3]
Механизм совместного восстановления ионов рения и вольфрама чрезвычайно сложен и пока недостаточно изучен. [4]
Добавление уксусной кислоты увеличивает только Rf ионов рения, а при добавлении соляной кислоты возрастает подвижность всех ионов. Для идентификации рения, молибдена и вольфрама удобнее применять смеси двух спиртов в присутствии уксусной и соляной кислот. [5]
 |
Результаты анализа эпитаксиальноп кремниевой пленки. [6] |
Как видно из таблицы, малый вклад ионов рения в полный ионный ток приводит к тому, что большинство содержавшихся в нем примесей ( Al, Si, Cl, Cu. Zn n In) оказываются за пределами обнаружения при анализе кремния. Холостая поправка в основном определяется примесями Na, Mg, К, Са ( концентрация которых в исследуемых пробах обычно гораздо выше), а также W, Мо, Та и Nb, как правило, не содержащимися в полупроводниковых веществах. [7]
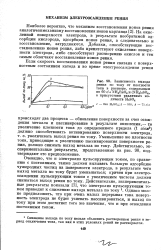 |
Зависимость выхода рения по току от плотности тока в растворе, содержащем по 60 г / л NH4Re04 и ( NH4 2S04, в присутствии различных количеств Ш804. [8] |
На окисленной поверхности электрода, в результате необратимой адсорбции кислорода, адсорбция ионов рения, а следовательно и восстановление, затрудняются. Добавки, способствующие восстановлению ионов рения, либо препятствуют окислению поверхности электрода, либо способствуют растворению окислов и тем самым облегчают восстановление ионов рения. [9]
При применении в качестве подвижной фазы ацетона или метил-этилкетона на слое окиси алюминия перемещается только ион рения. [10]
При применении в качестве подвижной фазы ацетона или метил-этилкетона на слое окиси алюминия перемещается только ион рения. При объемном отношении ацетон: вода, начиная с 1: 3, молибден также перемещается со стартовой линии. Только при прибавлении раствора соляной кислоты к кетонам ионы рения, молибдена, ванадия начинают одновременно перемещаться. Доны же вольфрама перемещаются при большом избытке кислоты. [11]
Низкий выход рения по току не может быть обусловлен низким перенапряжением выделения водорода и высоким перенапряжением восстановления ионов рения, поскольку при значительном увеличении концентрации ионов водорода ( при изменении рН от 5 5 до 1) выход водорода по току не только не увеличивается, а наоборот, уменьшается. [12]
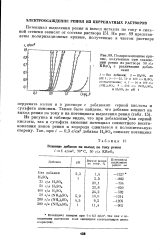 |
Поляризационные кривые, полученные при осаждении рения из раствора 50 г / л KRe04 с различными добавками. [13] |
Из рисунка и таблицы видно, что при добавленииткак серной кислоты, так и сульфата аммония потенциал совместного восстановления ионов рения и водорода сдвигается в положительную сторону. [14]
Было установлено, что в растворах смеси двух спиртов с увеличением количества спирта, имеющего меньший молекулярный вес, повышается величина Rf ионов рения. Добавление уксусной кислоты увеличивает только Rf ионов рения, а в случае соляной кислоты повышается подвижность всех ионов. Удобнее применять смеси двух спиртов в присутствии уксусной и соляной кислот для идентификации ионов рения, молибдена и вольфрама. [15]
Страницы: 1 2