Ион - роданид
Cтраница 2
При определенных условиях образует с соединениями шестивалентного молибдена в отсутствие или в присутствии ионов роданида характерные кристаллы [50, 157, 1041, 1245, 1503], используемые для микрокристаллоскопическо-го обнаружения молибдена. [16]
При определенных условиях образует с соединениями шестивалентного молибдена в отсутствие или в присутствии ионов роданида характерные кристаллы [50, 157, 1041, 1245, 1503], используемые для микрокристаллоекопическо-го обнаружения молибдена. [17]
Таким образом было найдено значение г 5 5 А для среднего расстояния между ионом роданида и электрическим центром тяжести системы. Если допустить, что остаточный эффект имеет отрицательную величину, то получим меньшее и более вероятное значение для этого расстояния. Меллер приводит значения трех констант устойчивости роданидных комплексов железа ( III), которые удовлетворяют с достаточной точностью его измерениям экстинкции. Однако автор настоящей работы полагает, что это не доказывает правильности предположения Мел-лера, поскольку в системах с более чем двумя комплексами в заметных концентрациях невозможно вычислить с достаточной точностью и константы и неизвестные молярные коэффициенты экстинкции присутствующих соединений. Так как Меллер пренебрег комплексами с более чем тремя ионами роданида, то, по-видимому, дироданидному комплексу приписана вообще слишком широкая область существования. [18]
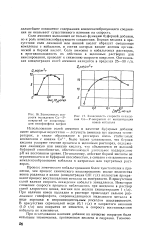 |
Зависимость ско - ри (. 7 Зависимость скорости осажде. [19] |
Процесс химического кобальтирования более чувствителен к примесям, чем процесс химического никелирования: малые количества ионов роданида и циана ( концентрация 0 01 г / л) полностью прекращают процесс восстановления металла на поверхности. В присутствии солей кадмия скорость осаждения кобальта замедляется. При наличии ионов палладия в растворе происходит сильное разложение гипофосфита, сопровождающееся выделением металла в виде порошка и непроизводительным расходом восстановителя. В присутствии сернокислой меди ( 0 1 г / л) и хлористого аммония ( 1 0 г / л) вид покрытия не меняется, и скорость восстановления кобальта не изменяется. [20]
Таким о: бразом было найдено значение г 5 5 А для среднего расстояния между ионом роданида и электрическим центром тяжести системы. Если допустить, что остаточный эффект имеет отрицательную величину, то получим меньшее и более вероятное значение для этого расстояния. Меллер приводит значения трех констант устойчивости роданидных комплексов железа ( III), которые удовлетворяют с достаточной точностью его измерениям экстинкции. Однако автор настоящей работы полагает, что это не доказывает правильности предположения Мел-лера, поскольку в системах с более чем двумя комплексами в заметных концентрациях невозможно вычислить с достаточной точностью и константы и неизвестные молярные коэффициенты экстинкции присутствующих соединений. Так как Меллер пренебрег комплексами с более чем тремя ионами роданида, то, по-видимому, дироданидному комплексу приписана вообще слишком широкая область существования. [21]
Метод основан на взаимодействии в сильно кислой среде ионов железа i ( III) с ионами роданида. [22]
Восстановление протекает на холоду в 1 0 - l 5N H2SO4 - Нитрат одновалентной ртути в отсутствие ионов роданида не восстанавливает шестивалентного молибдена. [23]
Изучена реакция взаимодействия тетраметилдиампноди-фенилантипирил карбинола и диметилднбензилдиаминодифе-нилантипнрплкарбииола с цинком, железом, кобальтом и другими элементами в кислой среде в присутствии ионов роданида. [24]
Помимо устойчивости окраски, ацетон увеличивает ее интенсивность, подавляя диссоциацию роданидного комплекса, и способствует замещению молекул воды вокруг иона металла ионами роданида. С малыми концентрациями роданида кобальт в присутствии адекватных количеств ацетона, этилового спирта или подобных растворителей не дает голубого окрашивания. [25]
Посторонние вещества попадают в раствор в виде примесей к основным реагентам, и при корректировании раствора концентрация этих примесей может быть столь значительной, что вредно отразится на процессе Данные исследования ( 1 ] показывают, что ничтожные количества ионов роданида и хлористого свинца ( 0 1 г / л) полностью прекращают процесс как в кислых, так и в щелочных никелевых растворах. Вредное влияние на процесс оказывают соли кадмия, причем в щелочных никелевых растворах в большей степени, чем в кислых никелевых Присутствие в кислом растворе хлористых солей цинка, магния, алюминия, железа н натрия ( до 0 1 г / л) не оказывает заметного влияния на процесс. [26]
При изучении влияния концентрации пятивалентного молибдена на образование роданидных соединений пятивалентного молибдена получены данные [220], которые позволяют считать, что в среде 2 N H2SO4 пятивалентный молибден при концентрации около 10 - 2 мол / л вступает в реакцию комплексообра-зования с ионами роданида в виде димерных форм. Понижение концентрации молибдена и повышение кислотности раствора приводит к деполимеризации катионов молибдена. [27]
При изучении влияния концентрации пятивалентного молибдена на образование роданидных соединений пятивалентного молибдена получены данные [220], которые позволяют считать, что в среде 2 N H SCU пятивалентный молибден при концентрации около 10 - 2 мол / л вступает в реакцию комплексообра-зования с ионами роданида в виде димерных форм. Понижение концентрации молибдена и повышение кислотности раствора приводит к деполимеризации катионов молибдена. [28]
Ионы роданида характеризуются восстановительными свойствами; в сильнокислых растворах они восстанавливают шестивалентный молибден до пятивалентного с образованием интенсивно окрашенных роданидных соединений. [29]
Ионы роданида характеризуются восстановительными свойствами; в сильнокислых растворах они восстанавливают шестивалентный молибден до пятивалентного с образованием интенсивно окрашенных роданидных соединений. [30]
Страницы: 1 2 3 4