Ион - рубидий
Cтраница 4
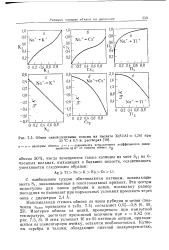 |
Обмен одновалентными ионами на цеолите X ( Si / Al 1 26 при 25 С в 0 1 н. растворах. [46] |
С наибольшим трудом обмениваются катионы, занимающие места Sj, локализованные в гексагональных призмах. Эти центры недоступны для ионов рубидия и цезия, поскольку размер последних не позволяет при нормальных условиях проникать через окна с диаметром 2 4 А. [47]
В связи с тем, что подвижности различных ионов в безводном гидразине неизвестны, нельзя было воспользоваться мостиком из раствора соли; вместо этого соединение двух полуэлементов осуществляли при помощи стеклянного шлифа. Было высказано предположение, согласно которому ион рубидия сольватируется очень слабо ( если он вообще сольватируется), в связи с чем отпадает необходимость введения поправки на энергию сольватации в процессе перехода металла в раствор в виде иона. [48]
Осадки хлороплатинатов калия, рубидия и цезия Me2 [ PtCl6 ] имеют желтый или оранжевый цвет, Хлороплатинаты рубидия и цезия менее растворимы, чем хлороплатинат калия. Насыщенным водным раствором хлороплатината калия обнаруживают ионы рубидия и цезия в присутствии ионов калия. [49]
В газообразном состоянии влияние структуры иона аммония становится более резко выраженным. В кристаллическом состоянии вращающийся ион аммония напоминает ион рубидия: он имеет такой же самый кажущийся размер, и из табл. 20 и 28 видно, что NH4I, имеющий структуру хлористого натрия, имеет почти такую же энергию решетки, как Rbl. Энергии решеток других аммонийных солей, не имеющих структуры хлористого натрия, за исключением фтористого аммония, также не сильно отличаются от энергий солей рубидия. [50]
В действительности Эйзенман рассматривал пять катионов щелочных металлов: Li, Na, К, Rb и Cs - и получил 11 рядов. По причинам, изложенным ранее, мы не рассматриваем ион рубидия. [51]
Образующийся осадок фосфата циркония отделя-с ют и высушивают. Так, при помощи фосфата циркония можно легко разделить ионы рубидия и цезия. [52]
Исследования влияния неводных растворителей на высоту полярографических волн папаверина, который восстанавливается в молекулярной форме, показали, что и в этом случае изменение высоты волны связано только с изменением коэффициента диффузии. Такие же результаты наблюдались нами и для некоторых ионов ( ионы рубидия и хинолина), мало сольватированных и мало изменяющих степень сольватации под влиянием растворителей. Гентери получил такие же простые соотношения для иона талия в этиленгликоле. Но уже для ионов натрия в смесях этилового спирта с водой не выполняется правило г дИф / т; const, что, вероятно, является следствием изменения сольватации этих ионов. Этим же, по-видимому, объясняется наблюдавшееся Перачио и Мелох различное изменение высот волн ряда щелочных металлов при переходе к неводным растворителям. [53]
Случаи положительной энтропии активации диффузии неоднократно наблюдали в исследованиях по сорбции. Рис и Рао [79] дают следующее возможное объяснение наблюдаемому эффекту: ион рубидия с диаметром 2 96 А, вследствие взаимодействия с кристаллической решеткой цеолита, помещается в центре узкого прохода ( окна), имеющего диаметр 2 8 А, в канале цеолита. Вызванная этим местная деформация кристаллической решетки вызывает ограничения свободы колебаний атомов кислорода, образующих окно, и самого иона, что и приводит к возникновению положительной энтропии активации. [54]
Можно думать, что ферроцианиды, имеющие диаметр внутри-структурных пустот порядка 3 - 3 5 А [1374], не могут цеолитно поглощать соли, анионы которых в силу своих размеров ( например, эффективные диаметры анионов S04a - x 4 6 А и J - ж 4 4 А) превышают диаметры каналов ферроцианидной сетки. Кроме того, в решетке ионообменно насыщенного ферроцианида все пустоты уже заняты ионами рубидия, компенсирующими заряд сетки. Это также должно препятствовать вхождению в такую решетку нейтральных молекул. [55]
Выбор потенциала водородного электрода в качестве нулевой точки при измерениях электродных потенциалов в различных растворителях является чисто условным. Тем не менее, следует ожидать, что свободная энергия будет изменяться при переносе иона рубидия из одного растворителя в другой даже в отсутствие значительной сольватации, если отличаются значения диэлектрической проницаемости растворителей. Составляющая свободной энергии, отвечающая переносу иона, в первом приближении обратно пропорциональна ионному радиусу и, по-видимому, незначительна для очень больших ионов. Стрелов [55, 56] при вычислениях с использованием видоизмененного уравнения Борна принимал в расчет возникающие по этой причине различия в стандартном потенциале. [56]
Страницы: 1 2 3 4