Ион - определяемое вещество
Cтраница 1
Ион определяемого вещества переводят при этом в подходящее комплексное соединение и экстрагируют, применяя неполярный растворитель. Этот метод применяют обычно в сочетании с последующим фотометрическим определением, так что его называют методом экстракционной фотометрии. [1]
Для того чтобы ионы определяемого вещества перемещались к индикаторному электроду только вследствие диффузии, а не за счет диффузии и электростатической силы притяжения ( миграционный ток), в исследуемый раствор добавляют какой-либо индифферентный электролит с катионом, восстанавливающимся гораздо труднее анализируемого катиона, например КС1, KNO3, NH4C1, при концентрации в 100 - 1000 раз превышающей концентрацию определяемого вещества. Такой электролит называется фоном. [2]
В исходном растворе находятся ионы определяемого вещества. По мере титрования содержание ионов в растворе меняется. Ионы одних соединений образуют малодиссоциирующие вещества, ионы других - нерастворимые соединения. В результате химической реакции в растворе появляются ионы, обладающие иной подвижностью. [3]
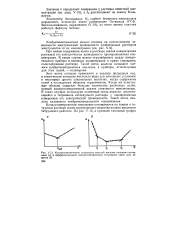 |
Кондуктометрическое титрование сильной кислоты сильным основанием ( а и дифференциальное Кондуктометрическое титрование смеси трех веществ ( б. [4] |
Кондуктометрическое титрование основывается на замене в титруемом растворе ионов определяемого вещества ионами вводимого титрующего реагента. [5]
К сожалению, допущение, что активность и концентрация идентичны, может привести к ошибкам в несколько процентов, особенно если ионы определяемого вещества многозарядны. [7]
 |
Кривые амперометрического титрования с двумя индикаторными электродами.| Кривая амперометрического титрования, построенная без учета разбавления. [8] |
При амперометрическом титровании следует особое внимание уделять выбору полярографического фона, учитывая возможные побочные химические реакции, связанные с изменением равновесия химической реакции титрования и состояния ионов определяемого вещества и титранта в растворе. [9]
 |
Кривые амперометрического титрования с двумя индикаторными электродами.| Кривая амперометрического титрования, построенная без учета разбавления. [10] |
При амперометрическом титровании следует особое, внимание уделять выбору полярографического фона, учитывая возможные побочные химические реакции, связанные с изменением равновесия химической реакции титрования и состояния ионов определяемого вещества и титранта в растворе. [11]
Для того чтобы ионы определяемого вещества перемещались к индикаторному электроду только вследствие диффузии, а не за счет диффузии и электростатической силы притяжения ( миграционный ток), в исследуемый раствор добавляют какой-либо индифферентный электролит с катионом, восстанавливающимся при более отрицательных потенциалах, чем анализируемый катион, например КС1, KNO3, NH4C1, при концентрации, в 100 - 1000 раз превышающей концентрацию определяемого вещества. Такой электролит называется фоном. [12]
Радиометрическое титрование основано на изменении в процессе титрования активности радиоактивного излучения ( радиоактивности) какого-либо компонента исследуемой системы. Такими компонентами могут быть ионы определяемого вещества А или реагента В, а также продукты реакции или специально вводимый в титруемый раствор радиоактивный индикатор. На различных этапах титрования измеряемая активность пропорциональна количеству фиксируемого компонента. [13]
Если, однако, в анализируемый раствор добавить другую соль, разложение которой наступает при большей разности потенциалов, чем это требуется для определяемого вещества, то в переносе тока начинают принимать участие также ионы добавленной соли. Таким образом, доля участия ионов определяемого вещества в переносе тока уменьшается. [14]
Нелинейное изменение электропроводности раствора может иметь место с начала титрования на некоторой части кривой или на всем участке кривой до точки эквивалентности. Это объясняется тем, что в процессе реакций смещаются ионные равновесия и изменяются равновесные концентрации ионов определяемого вещества, еще не вступившего в реакцию. Например, при нейтрализации довольно сильной, но не полностью диссоциированнной кислоты ( р / Са1) сильным основанием в процессе реакции уменьшается степень ее диссоциации под влиянием образующейся соли. Электропроводность раствора при нейтрализации этой кислоты до точки эквивалентности нелинейно понижается. Другим примером может служить титрование солей слабых кислот ( или слабых оснований), подвергающихся сильному гидролизу. В зависимости от силы кислоты, образующей соль ( или основания), кривая титрования может быть изогнута только в начале титрования или на всем участке до точки эквивалентности. В некоторых случаях на кривых титрования до точки эквивалентности может наблюдаться пологий минимум, не имеющий аналитического значения, что рассмотрено ниже на конкретных примерах. Аналогичные явления наблюдаются и в других случаях. При этом реакция может протекать количественно, а излом кривой титрования в точке эквивалентности может быть резко выраженным. Перед точкой эквивалентности электроприводность изменяется линейно, если реакция протекает до конца. [15]
Страницы: 1 2
