Ион - определяемое вещество
Cтраница 2
Однако, кроме диффузионного тока, под влиянием возникающего между катодом и анодом электрического поля появляется так называемый миграционный ток, возникающий от движения ионов раствора к катоду. Так как миграционный ток зависит не только от концентрации ионов в растворе, но и от некоторых других факторов, то его сила не является пропорциональной концентрации ионов определяемого вещества. [16]
При амперометрическом титровании, как и в полярографии, в раствор добавляют электролит-фон. Вначале фоном служит избыток ионов определяемого вещества, а затем появляющиеся в растворе ионы вещества, образующегося в результате реакции. [17]
К раствору в электролизере, содержащему исследуемые ионы, добавляют из ыикробюретки раствор-осадитель, переводящий определяемые ионы в осадок. Вначале ( до добавления осадителя) при потенциале, превышающем потенциал восстановления или окисления этого нона, гальванометр показывает наличие тока, а именно предельного тока определяемых ионов. Если теперь, не изменяя потенциала, добавлять к раствору осадитель, то концентрация ионов определяемого вещества будет уменьшаться, а следовательно, будет уменьшаться и величина предельного тока. [18]
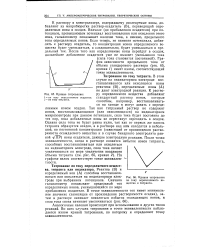 |
Кривые титрования.| Кривая титрования по току определяемого вещества и титранта. [19] |
К раствору в электролизере, содержащему исследуемые ионы, добавляют из микробюретки раствор-осадитель ( В), переводящий определяемые ионы в осадок. Вначале ( до прибавления осадителя) при потенциале, превышающем потенциал восстановления или окисления этого иона, гальванометр показывает наличие тока, а именно, предельного тока определяемых ионов. Если теперь, не изменяя потенциала, добавлять к раствору осадитель, то концентрация ионов определяемого вещества будет уменьшаться, а следовательно, будет уменьшаться и предельный ток. [20]
Следует отметить, что применение эквивалентов и нормальной концентрации имеет ряд недостатков. Для нахождения эквивалентов4 определяемого вещества и реагента необходимо составить уравнение данной реакции титрования. Однако если это сделано, более удобно расчеты вести непосредственно по этому уравнению с помощью молярных концентраций молекул, формульных единиц, ионов определяемого вещества и реагента. Кроме того, для многих веществ эквивалент изменяется при изменении условий протекания взаимодействия, даже при изменении рН раствора. Так, например, для перманганат-ионов в кислой среде г 5, в нейтральной т 3 и в сильнощелочной г - I. Поэтому одновременно с указанием эквивалента следует указывать также все условия, изменение которых может изменить величину эквивалента. К сожалению, не всегда это делается, и часто на практике пользуются найденным эквивалентом также для реакций с другими веществами, что приводит к неверным результатам. [21]
Такие соединения могут возникать в ходе химической реакции материала электрода с определяемыми ионами, например, при анодном растворении ртутного электрода в присутствии галогенид-ионов. Другой путь образования малорастворимых соединений - введение в раствор реагентов, которые образуют на поверхности электрода осадки с ионами металлов. В этом случае при электролизе ионы определяемого вещества восстанавливаются или окисляются на электроде до степени окисления, в которой они взаимодействуют с реагентом по реакции, приводящей к образованию осадка. Образовавшиеся соединения затем электрохимически окисляют или восстанавливают и измеряют ток. [22]
 |
Схема устройства простейшего капельного ртутного катода. [23] |
При рассмотрении процесса нами было принято, что число ионов металла в приэлектродном слое пополняется в результате диффузии. В действительности, если в растворе присутствуют только ионы анализируемой соли, то перенос тока от одного электрода к другому осуществляется ионами растворенной соли. Эти ионы под действием электрического тока передвигаются: к катоду-катионы и к аноду - анионы. Скорость движения ионов под действием электрического тока зависит от многих факторов: разности потенциалов между электродами, диаметра и заряда анализируемого иона, его концентрации в растворе и ряда других причин. Поэтому перенос ионов под действием электрического тока искажает процесс полярографического определения и сильно затрудняет проведение анализа. Однако если в анализируемый раствор добавлена другая соль, разложение которой наступает при большей разности потенциалов, чем это требуется для определяемого вещества, то катионы фона также движутся к катоду, но они не разряжаются при заданном потенциале. Таким образом, доля участия ионов определяемого вещества в переносе тока уменьшается. [24]
Страницы: 1 2