Ион - тетрабутиламмоний
Cтраница 1
Ион тетрабутиламмония почти количественно переносит цианид-ион из водной фазы в дихлорметан, а эмульгирование достигается с помощью специальной высокоскоростной мешалки. Одно из преимуществ использования эмульгированной системы состоит в высокой электропроводности электролитной среды, вследствие чего можно снизить прилагаемое к ячейке напряжение. Катализатор межфазного переноса обеспечивает протекание электродного процесса в органической фазе. Из 1 4 - ДМБ получается продукт замещения метоксигруппы - 4-метоксибензонит-рил с 40 % - ным выходом ( в расчете на вступившее в реакцию исходное соединение), а также примерно 3 % продукта замещения водорода - 2 5-диметоксибензонитрила. Аналогично 1 2 - ДМБ дает 2-метокси - и 3 4-диметоксибензонитрилы с выходами 26 и 11 % соответственно. [1]
 |
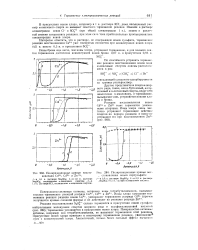
Зависимость a ( I4N для анионов л-динитробензола в этаноле от концентрации солей. [2] |
Для ионов тетрабутиламмония этот процесс не окончен еще и при концентрации 0 04 моль / моль. [3]
Здесь В - ион тетрабутиламмония, А - иодид-ион, а - водная и р - нитробензольная фазы. [4]
Координация атома азота в ионе тетрабутиламмония почти правильно тетраэдрическая. Расстояния N - С равны 1 53 - 1 59 А. [5]
 |
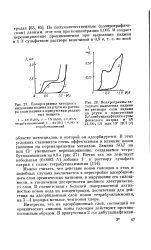
Окисление хромат-ионом. [6] |
Реакция гипохлорита с бензиловыми спиртами проводится в хлористом метилене или этилацетате и катализируется ионом тетрабутиламмония. При этом из первичных спиртов образуются альдегиды [ уравнение (11.6) ], а из вторичных - кетоны. [7]
Подобные явления наблюдаются при ускорении щелочного гидролиза метилнафтоата большими катионами, такими, как ион тетрабутиламмония, который, по-видимому, взаимодействует с субстратом и облегчает его атаку гидроксил-ионом; добавление больших анионов, таких, как тетрафенилборат, приводит к понижению скорости. [8]
Заметно перенапряжение водорода возрастает при адсорбции на поверхности металлических электродов положительно заряженных органических ионов, например иона тетрабутиламмония. В отличие от поверхностно активных анионов подобные вещества адсорбируются на отрицательно заряженной поверхности электрода и десорбируются при более положительных потенциалах по сравнению с точкой нулевого заряда. На перенапряжение заметно влияют добавки в электролит некоторых других высокомолекулярных соединений, коллоидов и слабых органических кислот. [9]
Реакция восстановления S2O - сильно тормозится в присутствии ионов сульфата нейтральными молекулами спиртов жирного ряда и сульфосалициловой кислотой ( рис. 284); торможение усиливается в присутствии ионов хлора. Поверхностно-активные катионы, например ион тетрабутиламмония, не вызывают торможения этой реакции Присутствие ионов хлора приводит к некоторому торможению реакции, усиливающее муся с концентрацией хлора. [11]
 |
Кривые сила тока-потенциал, получаемые при поляризации ртутного электрода в растворах, содержащих различные ионы. [12] |
Если вместо хлорида калия взять раствор другой соли, например хлорида лития, то область потенциалов горизонтального участка становится несколько шире ( около 2 1 в), а если взять раствор хлорида тетра-бутиламмония, то эта область расширяется почти до 2 6 в. Последнее объясняется тем, что реакции разрядов ионов лития, а в особенности ионов тетрабутиламмония, протекают при больших зарядах поверхности ( при более отрицательном потенциале), чем ионов калия. [13]
Можно считать, что действие ионов галоидов в этих и подобных случаях заключается в перестройке адсорбционного слоя органических катионов, в нарушении его сплошности, в увеличении дискретности двойного электрического слоя. В соответствии с большей поверхностной активностью ионов иода их концентрация, достаточная для действия на адсорбционный слой ионов тетрабутиламмония, на 3 - 4 порядка меньше, чем ионов хлора. [15]
Страницы: 1 2