Ион - фосфор
Cтраница 2
Концентрация фосфора в почвенном растворе стремится оставаться постоянной. По мере того как растения понижают эту концентрацию, поглощая требующийся им фосфор, часть ионов фосфора, адсорбированных почвенными коллоидами, переходит в раствор для восстановления нарушенного равновесия. [16]
Наконец, нам кажется важным отметить следующее обстоятельство. В ионе РО43 - фосфор имеет 5 положительных зарядов, в то время как в фосфиде ион фосфора имеет 3 отрицательных заряда. В процессе трансформации из положительного иона в отрицательный фосфор должен пройти через нейтральное, атомное состояние. В этом состоянии фосфор, вследствие способности к ассоциации в многоатомную молекулу и диффузии, может выйти из сферы реакции. [17]
Однако большая электроотрицательность фтора по сравнению с кислородом достаточна для того, чтобы сделать HF более сильной кислотой, чем вода, а вода является в свою очередь более сильной кислотой, чем аммиак. У фосфора в фосфине также имеется стремление поделить свои электроны, но в связи с большим размером иона фосфора действующие здесь силы настолько слабы, что фосфин в водном растворе не проявляет своих основных свойств в заметной степени. Однако известны соединения фосфония; эти соли разлагаются в воде, давая кислоту и фосфин. Более тяжелые элементы группы азота в периодической системе не образуют соединений такого типа. [18]
Следует отметить особенно положительное действие фосфора на физиологию растений: он ускоряет их рост и укоренение, что влечет за собой ускорение созревания. В главе VII мы узнали, что взаимодействию азота и фосфора благоприятствуют аммиачные формы удобрений, поскольку скорость проникновения ионов фосфора и аммония в клетки одинакова. Поэтому при местном внесении следует предпочесть аммиачную, а не нитратную форму азота. [19]
Предполагаемой особенностью структуры фосфатных стекол является наличие односторонне поляризованных кислородных ионов. Такие ионы возникают благодаря структуре тетраэдра Р04, где пятивалентный ион фосфора связан только с четырьмя ионами кислорода, отсюда один ион кислорода должен быть связан с ионом фосфора двумя связями. [20]
Существование чисто ионных связей атома фосфора убедительно не доказано. Даже в случае фосфидов щелочных металлов, свойства которых, как указывается в литературе, близки к свойствам обычных солей, результаты рентгенографических исследований3 21 не могут служить доказательством существования каких-либо ионов фосфора. Во всех тех случаях, когда тип связи в соединении был установлен с достоверностью, а не служил предметом умозаключений или предположений, было доказано, что связи фосфора с соседними атомами являются ковалентными. [21]
В нашем случае, где исследовалась электролитическая миграция радиофосфора в кристаллах хлорида калия при высокой температуре, анионная часть решетки тоже подвижна и поэтому эффективный заряд радиофосфора отражает взаимодействие ионов фосфора как с катионной, так и с анионной частью решетки. Таким образом, отрицательный эффективный заряд ( ЭФФ - - 0.2 е, где е - абсолютная величина заряда электрона) отнюдь не указывает на то, что фосфор находится в кристаллах хлорида калия в электроотрицательном состоянии, а лишь на то, что наблюдается достаточно сильное взаимодействие ионов фосфора с анионной частью решетки, так сказать увлекающей его при своем перемещении к аноду. [22]
Отдельно учитывают растворимость в 2 % - ной лимонной кислоте ( реактив Вагнера) - специальном реактиве, применяемом для сравнения растворимости разных шлаков. Эта градация растворимости, принятая чисто условно, применяется более полувека. Кроме того, пытались уточнить эффективность использования разных форм фосфора, рассуждая следующим образом: так как целью удобрения фосфором является повышение содержания ионов фосфора в почвенном растворе до 0 5 - 1 мг / л ( уровень, считающийся оптимальным), то фосфорные удобрения должны иметь растворимость гораздо выше 1 мг / л для того, чтобы они были способны достаточно быстро повысить концентрацию почвенного раствора. [23]
 |
Установка для ионного внедрения примесей в полупроводник. [24] |
При ионном методе внедрения примесей кремний покрывают слоем окисла, наносят электроды затвора, а затем уже пластину облучают ионами высокой энергии. Металлический электрод полностью поглощает ионы, а на незакрытых участках ионы примеси проникают в глубь кристалла, образуя проводимость нужного типа. Ионы проникают в кремний на очень малую глубину. При энергии 100 кэВ ионы фосфора и бора проникают на 0 4 и 0 6 мкм, а при увеличении энергии до 1 МэВ - глубина проникновения увеличивается всего до 1 5 - 2 мкм. [25]
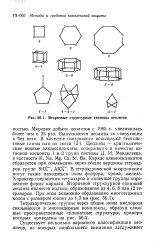 |
Вторичные структурные единицы цеолитов. [26] |
Выпускаются цеолиты со связующим и без него. В тетраэдрической координации могут также находиться ионы фосфора, хрома, железа. Характер соединения тетраэдров и конечные группы определяют форму каркаса. Вторичной структурной единицей цеолита является кольцо, образованное из 4, 6, 8 или 12 тетраэдров. [27]
 |
Окисление и окислительный аммонолиз пропилена. [28] |
В работе [347] изучена связь кислотно-основных свойств вис-мут-молибден-фосфориого катализатора и степени превращения на нем бутилена и бутадиена-1 3 в малешювый аилидрид. Рассмотрено взаимодействие ненасыщенных углеводородов ( являющихся слабыми основаниями), продуктов реакции ( имеющих кислотные свойства) и кислотно-основной поверхности катализатора. Показано, что на кислотной поверхности катализатора кислотные продукты реакции стабильны. Поэтому введение в молибдат висмута кислотных добавок ( ионов фосфора) увеличивает селективность окисления бутилена и - бутадиена-1 3 в малеиновый ангидрид: на кислотной поверхности катализатора ускоряется образование промежуточного л-аллильного комплекса, ведущего дальнейшее окисление. [29]
 |
Схема, иллюстрирующая образование возможного профиля примесей ( / из профилей для идеально беспорядочного ( 2 в. [30] |
Страницы: 1 2 3