Ион - цирконий
Cтраница 2
Полимеризация ионов циркония и гафния происходит одинаково. Основное различие сосюит в том, что при низкой кислотности ионы циркония более склонны к полимеризации и более высоко агрегированы по сравнению с ионами гафния. [16]
Малые содержания ионов циркония определяются по гашению люминесценции цирконий-моринового комплекса в результате взаимодействия с ионами фтора. Морин обладает собственным свечением, резко отличным от свечения циркониевого комплекса. Это позволяет полностью исключить свечение морина соответствующим подбором светофильтра. Комплексный ион фтора с ионом циркония не обнаруживает свечения. [17]
Минимальное количество ионов циркония, которое можно определить, составляет 5 - 6 мкг в 3 мл раствора. [18]
При осаждении ионов циркония из растворов добавлением аммиака или щелочи на холоду выделяется гидроокись ( или основная соль) в виде белого студенистого аморфного осадка. Гидроокись циркония образуется также при гидролизе некоторых солей циркония. Гидроокись циркония можно представить как гидратированную двуокись циркония, причем степень гидратации зависит от многих условий. При осаждении в щелочной среде на холоду образуется более гидратированный и высокодисперсный оксигидрат, чем при медленном гидролизе в слабокислой среде Яри нагревании. [19]
Реакция между ионами циркония и метилтимоловым синим в кислом растворе протекает очень медленно. Некоторые анионы, например, сульфаты, фториды и фосфаты катализируют эту реакцию, вероятно, благодаря лабилизации координационной сферы циркония. Важно заметить, что раствор соли циркония можно использовать в течение ограниченного периода времени. Определению сульфатов мешают многие катионы, но предварительное пропускание анализируемого раствора через колонку, заполненную катионообменной смолой, устраняет эти помехи. Мешающее действие эквимолярных концентраций мышьяка ( V), фторида и фосфата устраняется предварительной обработкой анализируемого раствора оксидом магния. [20]
Сероводород не осаждает ионы циркония и гафния из водных растворов. [21]
Купферон количественно осаждает ионы циркония и гафния из сернокислого раствора и применяется для отделения циркония от ряда элементов ( см. стр. [22]
В кислых растворах ионы циркония и фтора образуют ряд весьма прочных группировок. Окраска циркон-ализаринового лака ослабляется при введении фтора. На этом основаны многочисленные методы определения малых количеств фтора, даже связанных в прочные комплексы, например EF A, и в нерастворимых веществах, например CaF. [23]
Селенистая кислота осаждает ионы циркония из умеренно-кислых растворов в виде основного селенита, который при кипячении в присутствии избытка реагента переходит в кристаллический нейтральный селенит. Реагент может быть использован для отделения циркония от алюминия, таллия, титана, тория и редкоземельных элементов. [24]
Морин образует с ионами циркония внутрикомплексное соединение, структура которого окончательно не выяснена. Комплекс циркония с морином обладает интенсивной зеленой флуоресценцией, которая развивается в течение 10 - 15 мин. [25]
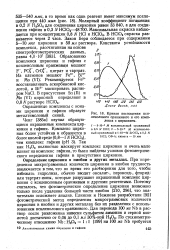 |
Кривая поглощения кси. [26] |
Окрашенные комплексы с ионами циркония и гафния образует метилтимоловый синий. [27]
В присутствии избытка реактива ион циркония количественно осаждается в азотно - или солянокислой среде в виде арсената циркония; титан сам по себе не осаждается, но при осаждении циркония он подвергается индуцированному осаждению даже при наличии в очень малых количествах. Образовавшийся осадок отфильтровывают и открывают в нем титан посредством перекиси водорода согласно реакции А. [28]
В полученном растворе открывают ион циркония так, как описано выше. [29]
Селенистая кислота количественно осаждает ионы циркония из солянокислых растворов в виде основного селенита. Селенистая кислота позволяет отделять цирконий от алюминия, некоторых редкоземельных элементов, небольших количеств железа, а при добавлении в раствор перекиси водорода - от небольших количеств титана. Торий и фосфор загрязняют осадок. [30]
Страницы: 1 2 3 4