Ион - гипохлорит
Cтраница 2
По этой же причине молекула окиси хлора очень лабильна и даже реакционную способность иона гипохлорита можно объяснить и связать с этим положением. [16]
 |
Концентрация Н0С1 и ОСЬ в воде при изменении величины рН. [17] |
Гипохлориты кальция или натрия, а также хлорная известь образуют в воде хлорноватистую кислоту и ион гипохлорита в соотношениях, определяемых рН водной среды. [18]
В три колбы добавляют соответственно 1, 3 и 5 мл стандартного раствора гипохлорита с содержанием иона гипохлорита 0 015 мг / мл. Доводят рН анализируемого раствора до 6 - 8 разбавленной соляной кислотой и добавляют определенный объем анализируемого раствора в четвертую колбу. [19]
Высокая степень кислотности или щелочности будет мешать образованию окрашенного соединения, как и присутствие какого-либо вещества, вызывающего восстановление ионов гипохлорита, хотя маловероятно, что эти обстоятельства возникают в большинстве проб воды. В соленых пробах помехи возникают в результате осаждения магния, когда комплексообразующая способность цитрата в реактивах превышена. Поэтому необходима предварительная дистилляция. [20]
Эпштейн с сотрудниками исследовал гидролиз зарина в хлорной воде при рН 5 - 9 и нашел, что гидролиз катализируется ионами гипохлорита. Скорость этой бимолекулярной реакции пропорциональна первой степени концентрации иона гипохлорита и зарина. Замена катионов, например калия или кальция, не оказывает влияния, так как в реакции принимает участие только ион гипохлорита. [21]
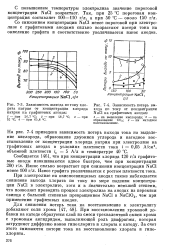 |
Зависимость выхода по току хлората натрия от концентрации хлорида натрия на графитовых анодах.| Зависимость потерь выхода по току от концентрации NaCl на графитовых анодах. [22] |
При восстановлении хромовой добавки на катоде образуется слой из смеси трехвалентной окиси хрома с хромовым ангидридом, выполняющей роль диафрагмы, которая затрудняет диффузию ионов гипохлорита и хлората к катоду. За счет этого снижаются потери тока на восстановление хлората и гипохлорита. [23]
Протеканию реакции по химическому механизму способствуют повышение концентрации NaCl в прианодном пространстве, поддержание рН на оптимальном уровне, увеличение температуры, затруднение процессов диффузии ионов гипохлорита к аноду и возможно быстрый вывод образовавшегося раствора гипохлорита и хлорноватистой кислоты из межзлектродного пространства электролитической ячейки. [24]
Осуществлению процесса по химическому механизму способствуют: повышение концентрации хлорида натрия в прианодном пространстве, увеличение - Температуры, поддержание рН на оптимальном уровне, затруднение процесса диффузии ионов гипохлорита к аноду. Образующийся в процессе хлорат остается в растворе, из которого его затем выделяют. [25]
Восстановление гипохлорита начинается при е0 0 86 В и хлората при е0 0 63 В. Ион гипохлорита восстанавливается легче иона хлората. [26]
Хлорноватистая кислота реагирует с аммиаком в воде, образуя монохлорампн NHjCl, дихлорамип NHCb и трихлорамин NC13 в зависимости от относительных количеств кислоты и аммиака. Хлор, хлорноватистая кислота и ион гипохлорита в совокупности характеризуют свободный остаточный хлор, а хлорамины - связанный остаточный хлор. [27]
Величина коэффициента п определяется для каждой реакции окисления цианидсодержащих соединений. При окислении цианидсодержащих сточных вод ионом гипохлорита окислитель может расходоваться не только на окисление цианидов, но и на окисление других веществ, присутствующих в сточных водах. [28]
Рассмотрим побочные реакции на катоде и катодной зоне. Помимо нейтрализации кислотности анолита на катоде происходит восстановление ионов гипохлорита, в которые переходит в щелочной среде хлорноватистая кислота, и ионов хлората. [29]
Эпштейн с сотрудниками исследовал гидролиз зарина в хлорной воде при рН 5 - 9 и нашел, что гидролиз катализируется ионами гипохлорита. Скорость этой бимолекулярной реакции пропорциональна первой степени концентрации иона гипохлорита и зарина. Замена катионов, например калия или кальция, не оказывает влияния, так как в реакции принимает участие только ион гипохлорита. [30]
Страницы: 1 2 3 4