Ион - дейтерий
Cтраница 1
Ионы дейтерия получают в ионном источнике, в котором молекулярный дейтерий, вводимый с помощью специальной системы, подвергают ионизации. [1]
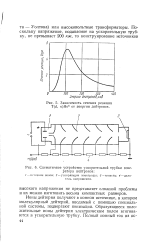 |
Зависимость сечения реакции T ( rf, He4 от энергии дейтронов.| Схематичное устройство ускорительной трубки генератора нейтронов. [2] |
Ионы дейтерия получают в ионном источнике, в котором молекулярный дейтерий, вводимый с помощью специальной системы, подвергают ионизации. Образующиеся положительные ионы дейтерия электрическим полем втягиваются в ускорительную трубку. [3]
Ионам дейтерия необходимая энергия сообщается в вакуумной ускорительной трубке. Для получения равномерного электрического поля вдоль трубки и для обеспечения хорошей фокусировки ионного пучка ускорительные трубки собирают из нескольких секций. Каждая секция состоит из электрода специальной формы и керамического изолятора. Обычно трубки низковольтных генераторов содержат четыре или более ускоряющих промежутка. В некоторых сильноточных нейтронных генераторах число ускоряющих промежутков сокращается до одного-двух. Напряжение на электроды ускоряющей трубки подается от высо-коомного делителя. [4]
В этих генераторах ионы дейтерия ускоряются до энергии 100 - 200 кэв и бомбардируют мишени из титана или циркония, насыщенные тритием. Нейтронные генераторы позволяют получить потоки нейтронов порядка 105 - 1010 нейтрон / ( см2 сек) и энергией - 14 Мэв. [5]
He 11 Принципиальна схема бомбардировки потоком ионов дейтерия ( дейтонов) или трития. [6]
При Т; 2 108 К тепловая скорость ионов дейтерия составляет примерно 10е ель / сек и за время. [7]
Как уже отмечалось, функция обратимости по отношению к ионам дейтерия стеклянного электрода в тяжелой воде имеет наклон, соответствующий теоретическому нернстовскому наклону почти во всей области кислотности, как и в случае водородного электрода в обычной воде. В частном сообщении Ритчи указал, что применение тяжелой воды в качестве растворителя внутри стеклянного электрода позволяет улучшить обратимость стеклянного электрода в окиси дейтерия. [8]
С этой точки зрения, электроды, стандартизованные по воде, не могут сразу применяться для прецизионных измерений активности иона дейтерия. [9]
Реакцию синтеза тяжелого и сверхтяжелого изотопов водорода ( 2Н 3Н 4Не п) изучают, налравляя ускоренные до энергии 2 МэВ ионы дейтерия на тритиевую мишень. Детектор регистрирует нейтроны, вылетающие перпендикулярно направлению пучка дейтонов. [10]
Реакцию синтеза тяжелого и-сверхтяжелого изотопов водорода ( Н2 Н3 п Не4) изучают, направляя ускоренные до энергии Е0 2 Мэв ионы дейтерия на тритиевую мишень. [11]
Реакцию синтеза тяжелого и сверхтяжелого изотопов водорода ( D2 T - He n) изучают, направляя ускоренные до энергии е02 МэВ ионы дейтерия на тритиевую мишень. Детектор регистрирует нейтроны, вылетающие перпендикулярно направлению пучка дейтонов. [12]
С и 2 73 при 100 С, то наблюдавшиеся при электролизе высокие коэффициенты разделения ( до 8) не могут быть объяснены установлением равновесия этой реакции на поверхности катода и, следовательно, должны быть результатом какого-то другого механизма; например, возможно, что на катоде ионы водорода легче отдают свой заряд, чем ионы дейтерия, вследствие чего у водорода появляется тенденция концентрироваться в газовой фазе. Это подтверждается и результатом лабораторных исследований [36]; было установлено, что коэффициенты разделения вплоть до 7 5 могут получаться в условиях необратимого электролиза при высоких плотностях тока или при наличии электродов, изготовленных из материалов, не катализирующих эту реакцию. [13]
Как и следовало ожидать, вода и окись дейтерия сходны по кислотно-основному поведению. Обратимый к ионам дейтерия, газовый дейтериевый электрод легко получается на платиновой поверхности, погруженной в тяжелую воду. Диэлектрические постоянные окиси дейтерия и воды весьма близки ( 77 9 для окиси дейтерия и 78 4 для воды при 25 С), тогда как плотность тяжелой воды ( 1 1 г / мл при 25 С) на 10 % выше плотности обычной воды. [14]
При электролизе воды или разнообразных водных растворов электролитов, на катоде разряжаются ионы водорода, покидающие электролизер в виде молекулярного водородного газа. Так же ведут себя и ионы дейтерия при электролизе тяжелой воды. Скорость катодного выделения водорода значительно превышает скорость выделения дейтерия. Поэтому при электролизе разбавленной тяжелой воды выделяющийся па катоде водород всегда значительно беднее дейтерием и богаче обыкновенным водородом, чем электролит в тот же момент. В результате этого, в ходе электролиза концентрация дейтерия в остатке жидкого электролита прогрессивно растет. [15]
Страницы: 1 2 3