Диффундирующий ион
Cтраница 2
Диаметр капилляров, возрастающий в направлении к золю, определяется типом диффундирующих ионов. Ширина капилляра зависит от степени гидро-фильности соединения, образующегося из диффундирующего иона и растворенного полиэлектролита. С увеличением гидрофильности этого соединения диаметр капилляров возрастает. Никель, кобальт и цинк способствуют образованию более широких капилляров при образовании геля альгината натрия, чем свинец, медь и кадмий. В этом случае возникает неориентированная структура геля без продольных капилляров. [16]
Будем считать, что диффузионный потенциал фд определяется разностью химических потенциалов диффундирующих ионов в обеих фазах. [17]
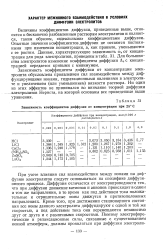 |
Зависимость коэффициентов диффузии от концентрации при 25 С. [18] |
Зависимость коэффициента диффузии от концентрации электролита обусловлена проявлением сил взаимодействия между диффундирующими ионами, гидратационными явлениями в электролите и увеличением ( или уменьшением) вязкости раствора. Ни один из этих эффектов не принимался во внимание теорией диффузии электролитов Нернста, на которой основаны все приведенные выше уравнения. [19]
 |
Изменение коэффициентов диффузии с концентрацией при 25 С. [20] |
Изменение коэффициента диффузии с концентрацией электролита объясняется, как результат проявления сил взаимодействия между диффундирующими ионами, гидратационных явлений в электролите и увеличения или уменьшения вязкости раствора. Ни один из этих эффектов не учитывался в теории диффузии электролитов Нернста, на которой основаны все приведенные выше уравнения. [21]
Если полимеры содержат ионогенные группы, то может происходить сильное взаимодействие этих групп с диффундирующими ионами, приводящее к сложному характеру диффузии. Примером подобного взаимодействия могут служить системы водных растворов электролитов - полиамиды. [22]
Матрица мембраны имеет заряд, ее проницаемость ограничивается или возрастает в зависимости от электростатического взаимодействия диффундирующих ионов с матрицей. Пример - ионообменные мембраны, применяемые для деминерализации. [23]
Разность электрических потенциалов, возникающая в месте контакта двух разнородных растворов, обусловленная различной подвижностью диффундирующих ионов. [24]
Дд - коэффициент диффузии; б - толщина диффузионного слоя; АС - разность концентраций диффундирующих ионов. [25]
Участок поверхности, на котором протекает адсорбция, приобретает заряд, знак которого совпадает со знаком диффундирующего иона. При адсорбции знак приобретаемого избыточного заряда совпадает со знаком медленно диффундирующего иона. Опираясь на правило, вывод которого дается ниже, можно качественно рассмотреть взаимодействия, обусловленные адсорбционным слоем, и предсказать направление процесса без детального математического анализа задачи. [26]
Из этого уравнения следует, что, в отличие от общей ионной концентрации, концентрация соли со свободно диффундирующими ионами ( NaCl) во внутренней жидкости всегда меньше, чем в наружной. [27]
При разделении мембраной коллоидного электролита от простого электролита, а также нормального электролита от смеси коллоидного и нормального электролитов свободно диффундирующие ионы распределяются неравномерно. Такое распределение впервые обосновал Доннан. [28]
Поскольку скорость процесса зависит в основном от диффузии и потому чрезвычайно резко растет с уменьшением расстояния, которое должны пройти диффундирующие ионы ( см. гл. X), то такие условия обеспечивают определяющую роль термодинамических факторов в разделении катионов. [29]
Вклад этих факторов в величины коэффициентов самодиффузии в различных условиях различен, зависит от природы и свойств ионита, растворителя и диффундирующих ионов, а также от ионного состава ионита. Количественная оценка их влияния в общем случае затруднительна. [30]
Страницы: 1 2 3 4