Соседний ион
Cтраница 1
Соседние ионы, включая и немагнитные, в особенности молекулы воды, создают в месте расположения рассматриваемого иона неоднородное электрическое поле. [1]
Соседние ионы, включая и немагнитные, и особенности молекулы воды, создают в месте расположения рассматриваемого иона неоднородное электрическое ноле. [2]
Соседние ионы Sjj - образуют в совокупности бесконечные спирали из атомов серы. [3]
Массы соседних ионов в строках таблицы отличаются на одну атомную единицу массы ( а. Таким образом, столбцы являются гомологическими рядами ионов. Табличное или графическое представление масс-спектров в виде набора гомологических рядов ионов хорошо соответствует основным направлениям распада молекул с углеводородным скелетом - разрыву С-С - связей. К ним относятся в первую очередь группы пиков ионов М, ( М - Н), ( М - R), положение и относительные интенсивности которых дают первое представление о группах соединений в смеси. [4]
При акустических колебаниях соседние ионы смещаются в одну и ту же сторону. [5]
В кристаллической решетке соседние ионы Na и С1 - по сравнению с изолированной молекулой NaCl обладают меньшим числом степеней свободы, поэтому тепловую энергию молекулы хлорида натрия можно рассматривать как ее максимальное значение для пары противоположно заряженных ионов в решетке. К запас ее тепловой энергии составляет 8 68 кДж - моль -, из которой всего лишь около 2 5 кДж - моль - приходится на колебательную энергию, непосредственно вызывающую распад молекул. Это количество термической энергии слишком мало по сравнению с тем, которое надо затратить на разрушение кристаллической решетки ( 762 кДж - моль -), чтобы обеспечить сколько-нибудь заметную диссоциацию хлорида натрия на ионы. [6]
В кристаллической решетке соседние ионы Na и С1 - по сравнению с изолированной молекулой NaCl обладают меньшим числом степеней свободы, поэтому тепловую энергию молекулы хлорида натрия можно рассматривать как ее максимальное значение для пары противоположно заряженных ионов в решетке. К запас ее тепловой энергии составляет 8 68 кДж - моль-1, из которой всего лишь около 2 5 кДж - моль-1 приходится на колебательную энергию, непосредственно вызывающую распад молекул. Это количество термической энергии слишком мало по сравнению с тем, которое надо затратить на разрушение кристаллической решетки ( 762 кДж - моль-1), чтобы обеспечить сколько-нибудь заметную диссоциацию хлорида натрия на ионы. [7]
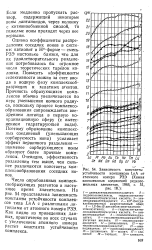 |
Зависимость константы устойчивости комплексов LnA от атомного номера РЗЭ ( Химия комплексных соединений редкоземельных элементов, 1966, с. 51, 18.. [8] |
Однако коэффициенты распределения соседних ионов в системе: катионит в Н - форме-смесь - РЗЭ настолько близки, что для их удовлетворительного разделения потребовалось бы огромное число теоретических тарелок колонки. [9]
Поскольку расчет влияния соседних ионов является задачей многих тел, общие формулы найти довольно трудно, однако некоторые приближенные выражения, справедливые при не очень низких температурах, могут быть получены. [10]
Для п п поля соседних ионов перекрываются и, следовательно, водородные состояния п п не существуют. [11]
 |
Радиальное распределение. [12] |
При этом поляризующее действие соседних ионов ( см. § 22) приводит к различного рода деформациям его. Разумеется, величину заряда иона следует понимать буквально только для однозарядных и в меньшей степени для двухза-рядных ионов. Ионы с более высокими зарядами едва ли встречаются в кристаллах, и в этих случаях надо понимат, что речь идет только об определенном состоянии атома данного элемента. Сопоставляя ионы ( или атомы), содержащие одинаковое число электронов в электронной оболочке ( С1 -, К), можно видеть, что те из них обладают меньшим размером, положительный заряд ядра которых больше. Вследствие этого анионы во всех случаях обладают значительно большими размерами, чем катионы, и в соответствии с этим анионы более легко поддаются деформации под действием соседних ионов и более легко поляризуются. [13]
Духовое состояние уменьшает заряд соседних ионов кислорода и тем самым изменяет их эффективный заряд. Проще всего рассмотреть это перераспределение заряда, если вернуться к - единственному гибридизованному состоянию кислорода и рассчитать перенос в наиболее сильно с ним связанное - состояние переходного металла доли электронов - [ WzlSWs ] 2 с каждым спином. [14]
Вероятность переноса электрона между соседними ионами, а следовательно, и вероятность возникновения полярных состояний возрастает. Оба рассматриваемых одноолектронных уровня перестают быть точно определенными, п вместо них возникают узкие зоны ( фиг. Если исходный более низкий уровень был полностью заселен, а более высокий - пуст, что соответствует ситуации, когда на один из рассматриваемых ионов, между которыми происходит перс-ход, приходится целое ( не разделяемое с другим ионом) число d - электроиов, вещество по-прежнему остается диэлектриком ( или соответственно полупроводником), п лишь величина энергии Eg, которая первоначально была равна энергии С /, слегка уменьшается. Однако кулоновская корреляционная энергия U все еще остается отличной от нуля, даже когда обе зоны перекрываются ( фиг. [15]
Страницы: 1 2 3 4