Тетраэдрический ион
Cтраница 2
Содержащие в своем составе тетраэдрические ионы РН [ d ( РН) 1 42 А ] соли фосфония представляют собой бесцветные кристаллические вещества. Перхлорат фосфония ( РН4СЮ4) весьма взрывчат, а галогениды при нагревании возгоняются, причем в парах они практически полностью диссоциированы на РН3 и соответствующий галоидоводород. [16]
Эта структура состоит из тетраэдрических ионов Ве ( Н О) 4 ] 2 и ионов SO J -, расположенных приблизительно таким же образом, как ионы в структуре хлористого цезия. [17]
Адсорбционная емкость лимитируется плотной упаковкой тетраэдрических ионов SO4 - - во внешней среде. [18]
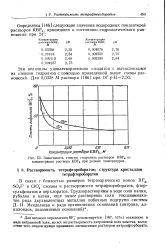 |
Зависимость степени гидролиза растворов KBF4 от концентрации раствора K. BF4 при разных температурах. [19] |
В связи с близостью размеров тетраэдрических ионов BF, SO8F и СЮ4 сходны и растворимости тетрафтороборатов, фтор-сульфонатов и перхлоратов. [20]
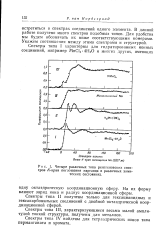 |
Четыре различных типа рентгеновских спектров К-края поглощения марганца в различных химических состояниях. [21] |
Спектры типа IV найдены для тетраэдрических ионов типа перманганата и хромата. [22]
Так, например, в тетраэдрическом ионе РО43 - каждая Р - О связь имеет длину 1 54 А, тогда как в Н3РО4 длина связи Р - ОН равна 1 57 А, а длина связей Р - О уменьшается до 1 52 А. Если вместо Н к кислороду присоединяется какой-нибудь органический радикал, то асимметрия становится значительно большей. Для серинфосфата, например, длина Р - О связи на стороне аминокислоты достигает 1 61 А с уменьшением длин других Р - О связей до 1 50 - 1 52 А. [23]
Существует множество довольно устойчивых кристаллических солей тетраэдрического иона аммония; большинство из них растворимо в воде, подобно солям щелочных металлов. [24]
Спектры указанных кристаллических веществ соответствуют колебаниям искаженных тетраэдрических ионов ХО, о чем свидетельствуют снятие вырождения ( полное или частичное) и изменение правил отбора. [25]
Как сказывается на устойчивости замена в тетраэдрическом ионе 5О4 - ато-ма кислорода на атом серы или пероксогруппу. [26]
С другой стороны, в структуре CsgCoCl6 имеются тетраэдрические ионы СоС1 -, непарные ионы С1 - и, конечно, ионы цезия. Соль с эмпирическим составом CsAuClg представляет интерес по многим причинам. Эта соль имеет черный цвет, тогда как CsCl бесцветен, а хлориды золота АиС13 и AuCl имеют оранжевую и желтую окраску соответственно. Как было сказано выше, эта соль содержит двухвалентное золото, но в соединениях такого типа глубокая окраска приписывается наличию элемента в двух различных валентных состояниях. Структура этого соединения тесно связана со структурой перовскита, в которой кристаллизуются многие фториды, например K. [27]
Ионные борогидриды ( например, NaBH4) содержат отдельные тетраэдрические ионы ВН4 -, причем структуры соединений МВН4 часто подобны структуре NH4C1, поскольку ионы NHJ и BHi изоэлектронны и обладают одинаковыми размерами. В LiBH4 тетраэдр ВН4 несколько искажен под действием притяжения маленького положительного иона Li, так что водородные атомы располагаются значительно ближе к этому атому. Тенденция к искажению увеличивается с ростом отношения заряда к радиусу катиона. В А1 ( ВН4) 3 каждая группа ВН4 имеет два атома Н, общие с атомом алюминия, и связь в группах А1 - Н - В можно описать трехцентро-вой МО, аналогичной МО в диборане. [28]
 |
Строение иона В3Н8. [29] |
Ионные борогидриды ( например, NaBH4) содержат отдельные тетраэдрические ионы ВН, причем структуры соединений МВН4 часто подобны структуре NH4C1, поскольку ионы NHJ и BHj изоэлектронны и обладают одинаковыми размерами. В LiBH4 тетраэдр ВН4 несколько искажен под действием притяжения маленького положительного иона Li, так что водородные атомы располагаются значительно ближе к этому атому. Тенденция к искажению увеличивается с ростом отношения заряда к радиусу катиона. В А1 ( ВН4) 3 каждая группа ВН4 имеет два атома Н, общие с атомом алюминия, и связь в группах А1 - Н - В можно описать трехцентро-вой МО, аналогичной МО в диборане. [30]
Страницы: 1 2 3 4