Рассматриваемый ион
Cтраница 2
Углекислый аммоний осаждает все рассматриваемые ионы. [16]
Если значение h для рассматриваемого иона или газа не известно, то можно использовать соответствующее значение для близкого компонента. [17]
Так как при взаимодействии рассматриваемых ионов с реагентом вытесняется два протона, взаимодействие по периоксихинон-ной группировке оказывается невозможным. Нетрудно показать по методу возмущений [3], как это было сделано в работе [6], что взаимодействие типа VII также не может иметь места, так как в этом случае должен был бы наблюдаться гипсохромный эффект. [18]
Поэтому получение окрашенного комплекса рассматриваемого иона с анионом слабой кислоты следует проводить при высоких значениях рН раствора. Однако нужно остерегаться резкого увеличения рН раствора вследствие возможности побочных процессов, ухудшающих колориметрическое определение: образования осадков гидроксидов или основных солей определяемого катиона. [19]
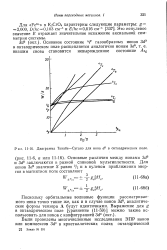 |
Диаграмма Танабе-Сугано для иона d3 в октаэдрическом поле. [20] |
Поскольку орбитальные волновые функции рассматриваемого иона точно такие же, как и в случае ионов 3d8, аналитические формы тензора Л будут идентичными. [21]
Из элементов, отвечающих рассматриваемым ионам, церий, торий и уран находятся в 3 - й группе периодической системы; цер. [22]
Из элементов, отвечающих рассматриваемым ионам, церий торий и уран находятся в 3 - й группе периодической системы; цер и относится к лантанидам, торий и уран - к актинидам; цирконий находится в 4 - й группе периодической системы. [23]
Из нее следует, что рассматриваемый ион имеет три набора связывающих и три набора разрыхляющих МО. Относительные энергии трех связывающих групп а - МО неизвестны. Указанный на рис. 113 порядок расположения МО основан на расчетах, которые в настоящей книге не приводятся. [24]
Известны и некоторые другие производные рассматриваемых ионов. Для аниона [ B20Hi8 ] 4 - установлено существование трех изомерных форм. [25]
Дьюар полагал, что в рассматриваемом ионе имеется дативная связь между парой я-электронов и мо-стиковым атомом; он считал, что о-электроны не способны к такой связи. [26]
Следовательно, при изучении кинетики переноса рассматриваемых ионов в области кислых и нейтральных растворов каких-либо ярко выраженных различий не было обнаружено. В связи с отсутствием значительных различий в свойствах изучаемых ионов их разделение в кислых и нейтральных средах при указанном расположении мембран и заполнении камер соответствующими растворами в нашей установке является практически неосуществимым. [27]
Особенность каталитического эффекта лиганда при электровосстановлении рассматриваемых ионов металлов проявляется в смещении волны в область положительных потенциалов и увеличение ее крутизны. Понятно, что то и другое очень важно в анализе. [28]
Дело в том, что между рассматриваемыми ионами, особенно ионами кальция, и водой существует очень сильное взаимодействие. Увеличение энтропии, обусловленное высвобождением молекул воды, связанных с этими ионами, намного превосходит уменьшение энтропии, обусловленное кристаллизацией. Эти эффекты графически изображены на рис. 1.15, из которого наглядно видно, какая закономерность проявляется в ряду карбонатов всех щелочноземельных металлов. Стоит обратить внимание, что ДЯ и Д5 по мере увеличения размера положительного иона одновременно уменьшаются, так как при этом ослабляется эффект гидратации. [29]
Это имело место в случае диметилтерефталата; рассматриваемые ионы образуются благодаря отрыву OR вместе с R и миграции одного атома водорода к заряженному осколку. Несмотря на то что этот пик обладает очень малой интенсивностью в спектре диметилтерефталата, в спектрах более тяжелых эфиров ( этиловых и выше) фталевой кислоты он часто бывает максимальным. Наличие подобного пика в спектрах большого числа фталатов приводит к выводу, что рассматриваемые ионы обладают высокой стабильностью. Один из путей образования этих ионов может быть установлен на основании изучения метастабильных пиков. [30]
Страницы: 1 2 3 4