Рассматриваемый ион
Cтраница 3
 |
Схема структуры NaCl ( к вычислению структурного коэффициента. [31] |
Далее, на расстоянии R 2 от рассматриваемого иона натрия расположены 12 ионов натрия. [32]
За этой первой координационной оболочкой степень упорядоченности структуры вокруг рассматриваемого иона быстро уменьшается, хотя некоторое подобие порядка и сохраняется во второй и еще в значительно меньшей степени - в третьей координационных оболочках. [33]
Потенциал р может зависеть только от расстояния г до рассматриваемого иона. [34]
Им было также установлено, что нарушение инги-бирующего действия рассматриваемых ионов при введении электролитов обусловлено каким-то специфическим эффектом, а не просто увеличением электропроводности раствора. [35]
За этой первой координационной оболочкой степень упорядоченности структуры вокруг рассматриваемого иона быстро уменьшается, хотя некоторое подобие порядка и сохраняется во второй и еще в значительно меньшей степени - в третьей координационных оболочках. [36]
А, - молекулярная электропроводность, п - число переноса рассматриваемых ионов, D определяется при Т577 К из равенства lgD lg Я-135. [37]
Во-первых, столкновения электронов ( а также ионов) с рассматриваемым ионом уменьшают время жизни иона в данном возбужденном состоянии. [38]
 |
Схема эффекта внедрения. [39] |
Анализ приведенных данных показывает, что колебания в величине термохимических радиусов рассматриваемых ионов обычно не превышают колебаний в величине ионных радиусов, найденных по данным рентгеноструктур-ного анализа. Вместе с тем обращает внимание наличие определенной зависимости величины термохимического радиуса аниона от размера катиона: с увеличением размера противоположно заряженного иона термохимический радиус данного несферического иона увеличивается. Изменение величины термохимического радиуса иона едва достигает 2 %, но наличие его несомненно. [40]
Постоянная Л определяется из условия, что в непосредственной близости от рассматриваемого иона потенциал целиком определяется им. [41]
Число частиц ( ионов, атомов или молекул), непосредственно окружающих рассматриваемый ион ( или атом), называется координационным числом. Так, в ионах ( SCU) 2, ( РС) 3, ( С1О4) - координационное число атомов серы, фосфора и хлора равно четырем, в ионах ( SO3) 2 -, ( СО3) 2 -, ( NO3) - координационное число серы, углерода и азота равно трем. [42]
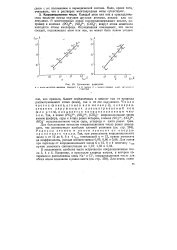 |
Сравнение радиусов. [43] |
Число частиц ( и оно в, атомов или молекул), непосредственно окружающих рассматриваемый ион ( или атом), называется координационным числом. Так, в ионах ( Р04) 3 -, ( SO4) 2 -, ( С1О4) - координационное число атомов фосфора, серы и хлора равно четырем, в ионах ( SOb) 2 -, ( СО3) 2 -, ( NO3) - координационное число серы, углерода и азота равно трем. [44]
Таким образом, вся совокупность изученных нами свойств позволяет считать, что сфера действия рассматриваемых ионов на воду имеет сравнительно большой радиус. Вместе с тем внешнесферное действие ионов по всей видимости отнюдь не носит чисто электростатический характер, поскольку на всех рисунках, изображающих термодинамические характеристики взаимодействия гексагидратов с водой ( рис. 12, 13, 14), зяметны индивидуальные особенности каждого электролита. Правда, в случае энтальпии, свободной энергии Д0т и энтропии Дчт растворения кристаллогидратов в воде эти особенности могут быть приписаны различным характеристикам кристаллических веществ. Однако учет данного обстоятельства не приводит к стиранию различий. Это видно из рис. 15, где представлены энтальпия А / / и свободная энергия ДО образования растворов из газообразных ионов М ( Н20) б и СЮГ и жидкой воды в зависимости от порядкового номера металла. Видно, что при всех концентрациях наибольший выигрыш Л / / и ДО сопровождает образование растворов перхлората никеля. [45]
Страницы: 1 2 3 4