Другой ион - металл
Cтраница 1
Другие ионы металлов в высших степенях окисления, вероятно, могут подобным же образом реагировать с аминами. [1]
Все другие ионы металлов связываются, кажется, только с фосфатной цепью. [2]
Расположить другие ионы металлов и порядке увеличения устойчивости их комплексов оказалось невозможным, поскольку необходимо учитывать природу лиганда. Точно так же невозможно расположить обычные лиганды и порядке их комплексообразующей способности, независимо от природы иона металла. [3]
С другими ионами металлов образуются аналогичные металлоцены, которые в большинстве своем, однако, менее устойчивы. [4]
С другими ионами металлов он не дает цветных реакций, при переходе в кислую область соединение с цинком разрушается. [5]
При замещении другими ионами металлов геометрия координации, подобная геометрии в Со ( П) - замещенном или нативном ферменте, не обязательно должна сохраняться. Это утверждение основывается на общих тенденциях координационной химии других катионов металлов и на результатах спектроскопических исследований. Исследование монокристаллов Си ( П) карбоксипептидазы Av методом ЭПР [223, 224] показывает, что в отличие от поля искаженных тетраэдрических комплексов поле лигандов иона Cu ( II) плоское. [6]
Цветных реакций с другими ионами металлов ( см. таблицу) в этих условиях формазаны не дают. [7]
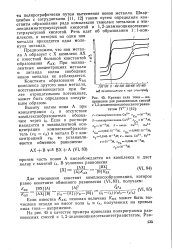 |
Кривые сила тока - напряжение для равновесных смесей с 1 2-диаминоциклогексантетрааце-татом ( Y4 -. [8] |
Константа образования Къх комплекса другого иона металла, восстанавливающегося при более отрицательном потенциале, может быть определена следующим образом. [9]
Иная картина наблюдается в растворах других ионов металлов, прежде всего ионов переходных элементов. В этом случае молекулы воды связаны с ионом сравнительно прочно и число их обычно равно шести или четырем. Связь воды с ионом металла носит ковалентный характер, даже если она сильно полярна. Таким образом возникают соединения высшего рода, называемые аквакомплексами ионов металла. [10]
Аналогичные исследования проводились и с комплексами других ионов металлов, но большинство данных получено все же для комплексов указанных выше четырех ионов. Это обусловлено чрезвычайной инертностью и нелабильностью по отношению к замещению большинства комплексов этих металлов. Нелабильные комплексы выбирают для исследования потому, что реакции с ними протекают достаточно медленно и их можно исследовать обычными методами классической кинетики. [11]
 |
Обмен перекиси кальция [ IMAGE ] Обмен перекиси бария с перекисью с перекисью водорода водорода. [12] |
Вероятно, аналогичным путем происходит окисление ряда других ионов металлов с переменной валентностью. Полученные данные не противоречат также механизму дегидрирования Мп ( ОН) 2 перекисью водорода. [13]
 |
Значения рН осаждения ионов некоторых металлов N-бензоилфенил-гидроксил амином.| Значение рН осаждения гидроксихинолинатов некоторых металлов. [14] |
Ионы марганца и хрома можно отделить от других ионов металлов переведением их в высшую степень окисления. При этом образуются хромат - и перман-ганат-ионы, которые хорошо растворимы в воде. [15]
Страницы: 1 2 3 4