Другой ион - металл
Cтраница 2
Интересно было бы найти индикаторные электроды, обратимые к другим ионам металлов; системы такого типа оказались бы - полезными для изучения ионного равновесия в растворе, особенно в тех случаях, когда нет иных обратимых металлических или амальгамных электродов. [16]
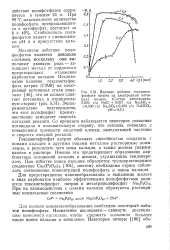 |
Влияние добавок гексамета-фосфата натрия на электродный потенциал железа. ( Состав электролита. 0 025 г / л N aCl 0 057 г / л Na2S04 0 530 г / л Na2SO3 0 420 г / л NaHC03. рН 9 2. [17] |
Гексаметафосфат натрия обладает способностью создавать с ионами кальция и другими ионами металлов растворимые комплексы, в результате чего ионы кальция, а также железа удерживаются в растворе. Именно это предотвращает образование карбонатных отложений кальция и железа, ухудшающих теплопередачу. При избытке ионов кальция образуется труднорастворимое соединение Са5 ( РзОюЬ [ Ю4 ], поэтому необходимо строго соблюдать соотношение концентраций полифосфата и ионов кальция. [18]
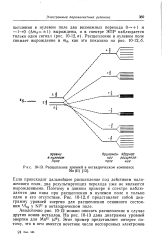 |
Расщепление уровней в октаэдрическом комплексе. [19] |
Аналогично рис. 10 - 12 можно описать расщепление в случае других ионов металлов. [20]
Металлический хром получается именно из прикатод-ной пленки; если в ней имеются другие ионы металлов, то они также восстанавливаются до металлического состояния. В пленке могут быть поры и разрывы, не пропускающие обычно используемые дисперсные частицы. Когда КЭП образуется из электролита хромирования, то частицы имеют сродство к пленке или же разрушают ее. [21]
Кроме того, ионы Мп2 и Cd3 ( а также и многие другие ионы металлов) связываются между этими двумя аминокислотами так, что парамагнитный зонд оказывается удачно расположенным в молекуле фермента. Соединение XXIX дает два хорошо различимых сигнала протонного магнитного резонанса от гликозидной и ацетильной метальных групп. Положение этих метальных групп относительно иона металла можно установить следующим образом. Наблюдаемый сигнал ЯМР для обеих групп представляет собой результат усреднения вкладов от комплексов лизоцим - XXIX, Cd3 - лизоцим - XXIX и от свободного соединения XXIX; концентрацией Cd 3 - XXIX можно пренебречь. [22]
Металлический хром получается именно из прика-тодной пленки; если в ней имеются другие ионы металлов, то они также восстанавливаются до металлического состояния. В пленке могут быть поры и разрывы, не пропускающие обычно используемые дисперсные частицы. Когда КЭП образуется из электролита хромирования, то частицы имеют сродство к пленке или же разрушают ее. [23]
При рН больше чем 4 - 4 5 сульфосалициловая кислота образует окрашенные комплексы с другими ионами металлов. [24]
Значительное возрастание объема связано с тем, что у карбоксильного катионита при обмене ионов водорода на натрий или другие ионы металлов происходит изменение ковалент-ной связи на ионную. [25]
Ацетоуксусный эфир образует темный красно-фиолетовый комплекс с хлоридом железа ( III), подобные же комплексы получаются со многими другими ионами металлов. Комплексы сходного строения с такими простыми кетона-ми, как ацетон, не обнаружены из-за низкой равновесной концентрации енола и нестабильности комплекса металла. [26]
Активность радикала оксалата способствует осуществлению механизма, при котором двухэлектронный лиганд окисляется одним ионом церия ( 1У) и другим ионом восстанавливающегося металла. [27]
Наиболее чувствительным из этих реагентов для меди является дитизон ( табл. 21), но с ним реагируют также многие другие ионы металлов, кроме меди. [28]
Экстракция урана аминами подобна его сорбции из соответствующих растворов анионообменными смолами; то же самое можно сказать и о поведении других ионов металлов. [29]
Тщательный контроль за концентрацией гидроксид-иояа часто приводит IK повышению селективности при осаждении гидрокоида или гидрата гидроксида одного катиона в присутствии другого иона металла. При таком относительно низком значении рН вероятность осаждения большинства гидроксидов двухз а рядных катионов металлов очень мала и может быть сведена к минимуму, хотя соосаж-дение все же будет иметь место. На практике удобно поддерживать значение рН около 4, используя ацетатный буфер, а также буферный раствор, содержащий пиридин и ион пиридиния. Преимущество последнего заключается в том, что пиридин образует устойчивые комплексы со многими двухзарядными ионами металлов, в результате чего уменьшается их соосаждение. [30]
Страницы: 1 2 3 4