Следующий инертный газ
Cтраница 2
При заполненном подуровне следует обратить внимание на числа электронов в различных уровнях ( слоях) у данного атома и числа электронов в соответствующих уровнях у атома предыдущего по порядковому номеру или ближайшего следующего инертного газа. [16]
При заполненном подуровне следует обратить внимание на числа электронов в различных уровнях ( слоях) у данного атома и числа электронов в соответствующих уровнях у атома предыдущего по порядковому номеру или у следующего инертного газа. [17]
При заполненном подуровне следует обратить внимание на числа электронов в различных уровнях ( слоях) у данного атома и числа электронов в соответствующих уровнях у атома предыдущего по порядковому номеру или у ближайшего следующего инертного газа. [18]
Но наряду с этим наблюдаются конфигурации d9s2 и d sp, расположенные относительно низко, в то время как соответствующие / 6s2 и p6sp у щелочных металлов не наблюдаются. Это и имеет место, хотя наши знания некоторых из этих спектров весьма отрывочны. Таким образом, мы доходим до следующего инертного газа, криптона, восемнадцатого элемента после предыдущего инертного газа - аргона. Они известны как первый большой период в периодической таблице. [19]
Одна из наиболее ранних удачных попыток объяснить образование химической связи за счет взаимодействия электронов принадлежит американскому физико-химику Дж. Согласно Льюису, каждый из двух атомов, вступающих в химическую связь, предоставляет в общее владение по одному электрону, так что пара электронов принадлежит одновременно двум атомам. При этом атомы стремятся достроить свои электронные оболочки по конфигурации следующего инертного газа. [20]
Природа связи металлоорганического катиона с анионом определяется потенциалами ионизации предельных структур, степенью долокализации заряда по аниону, легкостью деформации аниона и степенью перекрывания МО катиона и аниона. В большинстве случаев связи должны отличаться от чисто ионных, приближаясь скорее к комплексам со значительным переносом заряда, в которых на устойчивость существенное влияние оказывает величина расщепления МО, обусловленная перекрыванием. Для комплекса катион-анион с электронной оболочкой, превышающей по числу электронов оболочку следующего инертного газа, величина перекрывания имеет решающее значение, так как в этих комплексах электроны располагаются и на разрыхляющих молекулярных орбиталях. [21]
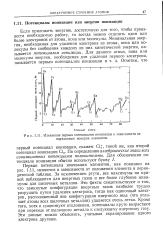 |
Изменение первых потенциалов ионизации в зависимости от порядковых номеров элементов. [22] |
Первые потенциалы ионизации элементов, как показано на рис. 1.11, меняются в зависимости от положения элемента в периодической таблице. За исключением ртути, все максимумы на кривой наблюдаются для инертных газов и все более глубокие минимумы для щелочных металлов. Эти факты свидетельствуют о том, что замкнутые конфигурации инертных газов наиболее трудно разрушить путем удаления электрона, тогда как одиночный электрон, расположенный вне конфигурации инертного газа ( что отличает атомы всех щелочных металлов) удаляется очень легко. Кроме того, хотя и существуют отклонения, потенциалы круто возрастают при переходе от щелочного металла к следующему инертному газу. Эти данные можно объяснить, учитывая экранирование одного электрона другими. [23]
Следующий инертный газ, криптон, имеет на 18 электронов больше, чем аргон. Можно было бы думать, что после образования двух восьми-электронных образуется оболочка с 18 электронами. В действительности дело обстоит иначе. Однако, чтобы это произошло, требуется 18 электронов, поскольку 10 из них располагаются на промежуточной оболочке, между третьей и четвертой оболочками. Доказательства в пользу такого заключения будут приведены при рассмотрении побочных подгрупп периодической системы, поскольку их образование теснейшим образом связано с построением промежуточной оболочки с 10 электронами. То же повторяется и у следующего инертного газа, ксенона. И он имеет на 18 электронов больше, чем криптон, из них только 8 располагаются на внешней, теперь уже пятой, оболочке, а 10 - на промежуточной оболочке между четвертой и пятой оболочками. И, наконец, радон имеет на 32 электрона больше, чем предшествующий инертный газ. Но и в этом случае во внешней оболочке находится только 8 электронов. Все остальные расположены на промежуточных оболочках, чем, между прочим, и объясняется, как будет показано позднее, появление подгруппы лантанидов. Итак, можно сделать вывод, что атомы всех инертных газов характеризуются наличием отличающейся особой устойчивостью внешней оболочки, которую в случае гелия образуют два, а у других инертных газов восемь электронов. [24]
Из теории Косселя следует, что характеристические свойства щелочных металлов определяются их местом в периодической системе. Они находятся в группе, непосредственно расположенной за инертными газами. Их нейтральные атомы содержат в соответствии с этим на один электрон больше, чем атомы предшествующих им инертных газов. Как показывают спектроскопические измерения работы ионизации, этот электрон легко отрывается, в то время как на отрыв второго электрона нужно затратить несравненно большую работу ( ср. Этим объясняется, почему щелочные металлы в своих гетеррполярных соединениях всегда положительно одновалентны. Невозможность получения соединений щелочных металлов которых они были бы отрицательно заряжены, объясняется слишком большим расстоянием каждого щелочного металла от следующего инертного газа. [25]
Из теории Косселя следует, что характеристические свойства щелочных 1 металлов определяются их местом в периодической системе. Они находятся в группе, непосредственно расположенной за инертными газами. Их нейтральные атомы содержат в соответствии с этим на один электрон больше, чем атомы предшествующих им инертных газов. Как показывают спектроскопические измерения энергии ионизации, этот электрон легко отрывается, в то время как на отрыв второго электрона нужно затратить несравненно большую работу ( ср. Этим объясняется, почему щелочные металлы в своих гете-рополярных соединениях всегда положительно одновалентны. Невозможность получения соединений щелочных металлов, в которых они были бы отрицательно заряжены, объясняется слишком большим расстоянием каждого щелочного металла от следующего инертного газа. [26]
Из теории Косселя следует, что характеристические свойства щелоч - ных металлов определяются их местом в периодической системе. Они находятся в группе, непосредственно расположенной за инертными газами. Их нейтральные атомы содержат в соответствии с этим на один электрон больше, чем атомы предшествующих им инертных газов. Как показывают спектроскопические измерения работы ионизации, этот электрон легко отрывается, в то время как на отрыв второго электрона нужно затратить несравненно большую работу ( ср. Этим объясняется, почему щелочные металлы в своих гетерополярных соединениях всегда положительно одновалентны. Невозможность получения соединений щелочных металлов, в которых они были бы отрицательно заряжены, объясняется слишком большим расстоянием каждого щелочного металла от следующего инертного газа. [27]
Страницы: 1 2