Двойной ион
Cтраница 1
Двойной ион ( например / б) может стабилизироваться двумя путями. [1]
Двойной ион ( например, 16) может стабилизироваться двумя путями. [2]
Однако такие факты, как, например, замещение в кристалле части Si двойным ионом Na Al, могут быть объяснены только с точки зрения определенных кристаллохимических представлений. Такого рода реакции замещения весьма распространены в природе, тогда как реакции замещения Si02 химически подобным ТЮ2 практически неизвестны. [3]
Бьеррум [20] считал, что заряды амфиона достаточно пространственно разделены и поэтому он проявляет свойства двойных ионов. [4]
Следует обратить внимание на то обстоятельство, что полученные здесь выводы относительно изоэлектрической точки сохраняют свое значение независимо от того, состоит ли нейтральный амфолит из двойных ионов ( амфионов) или из незаряженных молекул. Если значения k: и kz получены опытным путем, то они не зависят от предположений относительно природы обусловливающих их групп. Предыдущее изложение исходило из предположения, что нейтральной молекулой является RH, что действительно имеет место в случае алифатических аминокислот. [5]
Заметим, что эти величины определены для ионных пар, а не для ковалонтных частиц. Нейтральная молекула существует в растворе как бы в виде двойного иона, так что в этом случае возникает значительное ион-дипольное взаимодействие. [6]
Зам - тим, что эти величины определены для ионных пар, а не для ковалентных частиц. Нейтральная молекула существует в растворе как бы в виде двойного иона, так что в этом случае возникает значительно ион-дипольное взаимодействие. [7]
 |
Спектр поглощения акридинового оранжевого. [8] |
При этом происходит обратимое понижение полосы поглощения основного состояния, поскольку число молекул в основном состоянии уменьшается. Далее Цанкером было показано, что при повышенных концентрациях образуются двойные ионы, которые характеризуются измененным спектром поглощения и испускания. [9]
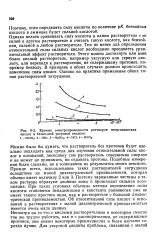 |
Кривые электропроводности растворов неорганических кислот в безводной уксусной кислоте. [10] |
Можно было бы думать, что растворитель без протонов будет идеально подходить как среда для изучения относительной силы кислот и оснований, поскольку сам растворитель совершенно инертен и не может ни принимать, ни отдавать протоны. Подобные измерения были сделаны, но в толковании их результатов много неясного. Поэтому заряженные частицы в таком растворе образуют двойные ионы и происходит сильная ассоциация. При таких условиях обычные методы определения силы кислоты становятся ненадежными и константа равновесия уже не имеет такого простого вида, как в растворителе с большой диэлектрической проницаемостью. Об относительной силе кислот и оснований в растворителях с малой диэлектрической проницаемостью имеется очень мало данных. [11]
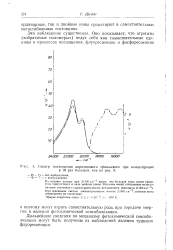 |
Спектр поглощения акридинового оранжевого при концентрации в 10 раз большей, чем на 3. [12] |
Эти ионы имеют собственное метаста-бильное состояние с характеристическим поглощением ( максимум 15500 с. При освещении светом, соответствующим полосе 21 500 г. к 1, двойные ионы распадаются на одиночные. [13]
 |
Относительная сила неорганических кислот, найденная по измерениям электропроводности их растворов в безводной уксусной кислоте. 1 - НС1О4. 2 - НВг. 3 - H2SO4. 4 - НС1 5 - HNO. [14] |
Однако нельзя сравнивать силу кислоты в одном растворителе с ее силой в другом растворителе и считать такую кислоту как бензойная, сильной в любом растворителе. Тем не менее для определения относительной силы сильных кислот необходимо преодолеть уравнительный эффект растворителя. В принципе, в обоих случаях должно происходить изменение силы кислот. Однако на практике применение обоих типов растворителей затруднено. Можно было бы думать, что растворитель без протонов будет идеально подходить как среда для изучения относительной силы кислот и оснований, поскольку сам растворитель совершенно инертен и не может ни принимать, ни отдавать протоны. Такого рода измерения были сделаны, но в толковании их результатов много неясного. Поэтому заряженные частицы в таком растворе образуют двойные ионы и происходит сильная ассоциация. При таких условиях обычные методы определения силы кислоты становятся ненадежными и константа равновесия уже не имеет такого простого вида, как в растворителе с большой диэлектрической проницаемостью. Об относительной силе кислот и оснований в растворителях с малой диэлектрической проницаемостью имеется очень мало данных. [15]
Страницы: 1 2