Противоположно заряженный ион
Cтраница 3
Взаимное притяжение противоположно заряженных ионов, в результате которого возникает молекула, носит электростатический характер. [31]
В реакциях противоположно заряженных ионов при образовании активированного комплекса заряд уменьшается. Это приводит к уменьшению электрострикции и к положительной энтропии активации. [32]
 |
Зависимость степени. [33] |
Взаимодействие двух противоположно заряженных ионов не приводит к полной взаимной компенсации их полей, они сохраняют способность притягивать и другие ионы. Поэтому в отличие от ковалентной ионная связь не обладает насыщаемостью. Из-за отсутствия у ионной связи направленности и насыщаемости каждый ион окружен ионами противоположного знака, число которых определяется размерами и силой отталкивания одноименно заряженных ионов. Поэтому соединения с ионной связью представляют собой кристаллические вещества. [34]
 |
Эффективные заряды гэф катионов в некоторых ионных кристаллах. [35] |
Расстояния между противоположно заряженными ионами в кристаллах меньше, чем расстояния между одноименными ионами, поэтому электростатические силы межионного притяжения преобладают над силами отталкивания. Так как электростатические силы не обладают ни насыщаемостью, ни направленностью, каждый ион взаимодействует не только с ионами своего непосредственного окружения, но и со всеми другими ионами кристалла. Рассмотренная картина электростатического межионного взаимодействия не учитывает того, что валентные электроны атомов частично обобществляются и связь не является чисто ионной. При этом, однако, эффективные заряды в ионных кристаллах всегда остаются большими. [36]
 |
Схема расположения.| Перераспределение электронной плотности в атомах водорода при их сближении. [37] |
Между двумя противоположно заряженными ионами возникает электростатическое взаимодействие, которое и приводит к образованию электровалентной ( ионной) связи. Молекулы, образованные электровалентной связью, являются диполями. В твердом состоянии они образуют кристаллы с ионными кристаллическими решетками, а в растворах подвергаются электролитической диссоциации. [38]
Коагуляция гидрозоля противоположно заряженными ионами электролитов существенно отличается у положительных и отрицательных золей. Согласно Фрейндлиху, коагуляцию следует понимать как наложение положительных или отрицательных ионов на поверхность противоположно заряженных частиц золя, в результате чего заряды взаимно нейтрализуются. Коагуляция почти точно совпадает с точкой, в которой частицы коллоида разряжаются и больше не мигрируют при электрофорезе. Наоборот, скоагулированные нейтральные частицы геля могут быть вновь заряжены путем наложения некоторых ионов, после чего агломерат снова перейдет в золь. Процесс перехода геля в золь называется пептизацией, В качестве примера могут служить гидрогели окиси алюминия, которые при прибавлении небольших количеств соляной кислоты, снова превращаются в суспен-зоидные золи. При этом только часть гидроокиси алюминия превращается в хлористый алюминий, которого оказывается достаточно для пептизации. [39]
При многовалентных противоположно заряженных ионах сразу идет быстрое падение до нуля, после чего происходит перезарядка поверхности. [41]
 |
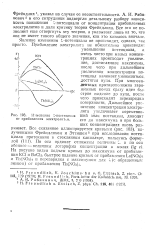
Зависимость потенциальной энергии от расстояния г между компонентами. [42] |
При ионной ассоциации противоположно заряженные ионы притягиваются за счет электростатического притяжения их свободных зарядов на расстояния, где ближние силы отталкивания становятся равными силам притяжения. На этом расстоянии потенциальная энергия их взаимодействия минимальна, что соответствует равновесному положению, которое может быть легко нарушено тепловой энергией. [43]
Образующиеся при этом противоположно заряженные ионы могут соединяться более или менее правильным образом и в соотношении, которое обеспечивает общую электронейтральность образующегося ионного соединения. Иными словами, между ионами существуют ионные связи. [44]
Главное действие производит противоположно заряженный ион. [45]
Страницы: 1 2 3 4 5