Положительно заряженный ион
Cтраница 3
Положительно заряженный ион С2Н6 образуется в состоянии Eg. Оба состояния, Еи и Eg, неустойчивы из-за эффекта Яна - Тел-лера, активным колебанием является Eg. Этот ион имеет, по-видимому, структуру симметрии С2л, нечто среднее между структурами С2Н6 и В2Нв, но ближе к первой. [31]
Положительно заряженные ионы обычно называют катионами, а отрицательно заряженные - анионами. Сам процесс распада ионной молекулы на отдельные ионы может быть представлен следующим образом. В положении А отрицательный конец диполя будет притягиваться к иону, а положительный отталкиваться. [32]
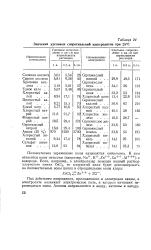 |
Значения удельных сопротивлений электролитов при 25 С. [33] |
Положительно заряженные ионы называются катионами. К ним относятся ионы металлов ( например, Na -, K - -, Zn - -, Си, А1 - - - - - -) и водорода. [34]
Положительно заряженные ионы, используемые в преобразователях, принципиально могут быть получены одним из следующих способов: газовым разрядом при пониженном давлении, высокочастотной искрой в вакууме, из раскаленных солей, ионизацией исследуемого газа медленными электронами и поверхностной ионизацией на раскаленном металле. [35]
Положительно заряженные ионы называют катионами, отрицательно заряженные - анионами. Отношение числа молекул, распавшихся на ионы, к общему числу растворенных молекул электролита называют степенью диссоциации. [36]
Положительно заряженные ионы называются кат ион а-м и, отрицательно заряженные ионы - а н и о н а м и. [37]
Положительно заряженные ионы называются катионами, отрицательно заряженные ионы - анионами. Проводящий раствор электрически нейтрален; в нем одновременно присутствуют и катионы, и анионы. [38]
Положительно заряженный ион ВЮ по всей вероятности сорбируется ионогенными группами. При рН выше 3 возникают условия, благоприятные для образования малорастворимых окисленных соединений висмута. [39]
Положительно заряженный ион кремния является в данном случае комплексообразователем, вокруг которого располагаются ионы фтора и нейтральные молекулы HF. Кремнефтористоводородная кислота существует только в водном растворе и имеет большую степень диссоциации. [40]
Положительно заряженный ион Ag обладает большим сродством к электрону, так как энергия, выделяющаяся при присоединении электрода к положительному иону, равна энергии ионизации с обратным знаком. Поэтому положительно заряженный ион Ag является сильным окислителем. Ион NO-T в данных условиях ни окислительных, ни восстановительных свойств проявлять не может. [41]
 |
Элементы трубчатого ( а и пластинчатого ( б электрофильтров ( электроосадителей ( вид сверху. [42] |
Положительно заряженные ионы воздуха быстро достигают отрицательного проволочного электрода и нейтрализуют на нем свой заряд. Электроны двигаются в направлении силовых линий электрического поля к положительному трубчатому электроду. Вдоль оси трубы перемещается запыленный газ, и свободные электроны, двигаясь поперек потока газа, сталкиваются с частицами ( как правило, состоящими из какого-либо диэлектрического вещества) и заряжают их поверхностным отрицательным зарядом. Получившие отрицательный заряд частицы начинают относительно медленно перемещаться вдоль силовых линий поля к положительному трубчатому электроду. Такое движение называют электростатическим осаждением пыли на внутреннюю поверхность вертикальной трубы. Отдав свой отрицательный заряд стальной трубе, частицы под действием силы тяжести перемещаются вниз вдоль внутренней стенки трубы, где собираются в коническом днище и выгружаются через секторный затвор. [43]
 |
Прибор для электрофореза Рабиновича и Фодиман.| Схема электроосмоса. [44] |
Положительно заряженные ионы диффузного слоя не связаны в своей подвижности и перемещаются под действием электрического поля вправо. Эти ио) ны, перемещающиеся вместе со своими гидратными оболочками, увлекают за обой окружающую их жидкость, что и наблюдается в процессе электроосмоса. [45]
Страницы: 1 2 3 4