Положительно заряженный ион - металл
Cтраница 1
Положительно заряженные ионы металлов и неметаллов, если они не проявляют высших степеней окисления равных номеру групп, в которых находятся элементы, могут быть восстановителями. [1]
Положительно заряженные ионы металлов и неметаллов, способные принимать электроны. [2]
Положительно заряженные ионы металлов взаимодействуют с электронами и разряжаются на поверхности покрываемых изделий ( в гальваностегии) или на поверхности спец. [3]
Положительно заряженные ионы металлов, способные переходить в ионы более высокой степени окисления, являются восстановителями. [4]
Между положительно заряженными ионами металла в кристаллической решетке существуют силы электростатического отталкивания. [5]
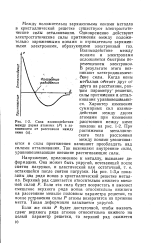 |
Сила взаимодействия между двумя атомами ( Р в зависимости от расстояния между ними ( х. [6] |
Между положительно заряженными ионами металла в кристаллической решетке существуют электростатические силы отталкивания. Одновременно действуют электростатические силы притяжения между положительно заряженными ионами и отрицательно заряженными электронами, образующими электронный газ. [7]
Катионы - положительно заряженные ионы металлов и водорода передвигаются к катоду. [8]
Таким образом, положительно заряженные ионы металла оказываются как бы погруженными в электронный газ ( рис. 5, б) у которого электроны находятся в квазисвободном состоянии. Ионы удерживаются вместе благодаря притяжению находящихся между ними валентных электронов. [9]
На анодных участках положительно заряженные ионы металла переходят в электролит ( грунтовые воды, грунт), вызывая разрушение металла. [10]
При коррозионном процессе положительно заряженные ионы металла переходят из узлов решетки кристаллов в коррозионную среду, где при последующих химических реакциях могут образовываться прочные соединения металлов. Таким образом, коррозионный процесс соответствует положительному току, току катионов металла в коррозионную среду. [11]
Обычно отрыв гидрид-иона положительно заряженным ионом металла или положительным концом приближающегося поляризованного мономера происходит у предпоследнего углеродного атома растущей цепи. Однако, поскольку несколько последних звеньев благодаря изгибу полимерной молекулы могут быть расположены рядом с комплексом, отрыв гидрид-иона может произойти у пятого или шестого от конца углеродного атома. В этом случае образуется циклическая концевая группа или внутренняя двойная связь. [12]
 |
Схема кристаллической решетки металлов. [13] |
Связь между всеми положительно заряженными ионами металлов и свободными электронами в кристаллической решетке металлов называется металлической связью. [14]
Обычно отрыв гидрид-иона положительно заряженным ионом металла или положительным концом приближающегося поляризованного мономера происходит у предпоследнего углеродного атома растущей цепи. Однако, поскольку несколько последних звеньев благодаря изгибу полимерной молекулы могут быть расположены рядом с комплексом, отрыв гидрид-иона может произойти у пятого или шестого от конца углеродного атома. В этом случае образуется циклическая концевая группа или внутренняя двойная связь. [15]
Страницы: 1 2 3