Молекулярный ион - кислород
Cтраница 2
Одноэлектронную волну, отвечающую стадии ( V), можно наблюдать при восстановлении кислорода на ртути в присутствии некоторых органических веществ или в апротонных растворителях, в которых молекулярный ион кислорода О достаточно устойчив. [16]
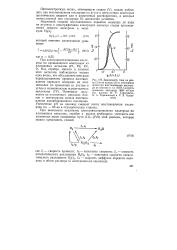 |
Зависимости тока на дис. [17] |
Одноэлектронную волну, отвечающую стадии ( V), можно наблюдать при восстановлении кислорода на ртути в присутствии некоторых органических веществ или в апротонных растворителях, в которых молекулярный ион кислорода Оз достаточно устойчив. [18]
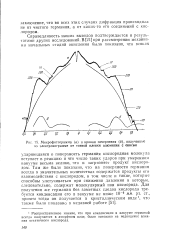 |
Микрофотограмма ( а и кривая почернения ( б, полученные по электронограмме от тонкой пленки алюминия с окисью. [19] |
Там же было показано, что на поверхности германия всегда в значительных количествах содержатся продукты его взаимодействия с кислородом, в том числе и такие, которые способны улетучиваться при снижении давления и которые, следовательно, содержат молекулярный ион кислорода. Для получения же германия без заметных следов кислорода требуется конденсация его в вакууме не ниже 10 - 6 мм. [20]
 |
Распределение электронов в атоме никеля ( о, в изолированном ионе Ni2 ( б, в и в ионах Mi24 -, входящих в тетраэдрический ( г и плоско-квадратный ( д комплексы. [21] |
Магнитные свойства молекулярных ионов кислорода ( О2 -, О2) и кристаллических соединений, ими образованных, подтверждают предложенные распределения электронов по молекулярным ор-биталям и хорошо согласуются с энергетическими свойствами ионов и межъядерными расстояниями. [22]
Кинетические закономерности восстановления кислорода в кислом и нейтральном растворах могут быть объяснены, если предположить, что замедленной стадией, определяющей скорость, служит первая. В щелочном растворе, напротив, эта стадия и последующее превращение молекулярного иона кислорода в радикал пергидроксила протекают в равновесных условиях, в то время как образование иона пергидроксила замедленно. [23]
 |
Энергетическая схема образования молекулы NO. [24] |
Дж / моль), где связь тройная. Вместе с тем, по энергии диссоциации молекула NO близка к молекулярному иону кислорода О. [25]
 |
Энергетическая схема образования молекулы NO. [26] |
Дж / моль), где связь тройная. Вместе с тем, по энергии диссоциации молекула NO близка к молекулярному иону кислорода OJ ( 644 кДж / моль), в котором кратность связи также равна 2 5 ( см. стр. [27]
Действительно, энергия диссоциации молекулы NO на атомы ( 150 ккал / моль) имеет промежуточное значение по сравнению с соответствующими величинами для молекулы О. Вместе с тем, по энергии диссоциации молекула NO близка к молекулярному иону кислорода Oz ( 154 ккал / моль), в котором кратность связи также равна 2 5 ( см. стр. [28]
Отсюда находим параметр гранецентрированной кубической решетки а 4 868 А. Принимая для радиуса иона цинка величину 0 72 А и замечая, что на половине длины ребра куба находится один ион цинка и один ион кислорода ( как в решетках типа хлористого натрия), находим для диаметра кислородного иона величину 3 43 А. Вопрос об ориентировке молекулярного иона кислорода остается пока открытым. [29]
Ни одна из высказанных гипотез до сих пор не получила достаточного экспериментального обоснования, и вопрос о том, проникают ли электрические заряды непосредственно в кровь ( пенетрационная гипотеза) или действуют на кровь путем электростатической индукции ( индукционная гипотеза), ждет своего исследователя. Однако автором и другими исследователями были получены доказательства электрохимических и электростатических сдвигов в системе крови, которые возникают под влиянием вдыхания униполярных аэроионов. Поэтому весьма вероятно, что молекулярный ион кислорода с несомым им зарядом непосредственно в процессе газообмена проникает в кровяное русло. [30]
Страницы: 1 2 3