Комплексный ион
Cтраница 1
Комплексные ионы обладают способностью диссоциировать в большей или меньшей степени с образованием более простых ионов. [1]
Комплексный ион работа зарядки 518 свободный, термы 495 центральный 377 Ионная пара 512 ел. [2]
Комплексные ионы во многих случаях дают новые, совершенно отличные характерные реакции. [3]
Комплексные ионы имеют свои особенные реакции, отличные от реакций катионов, анионов и нейтральных молекул, входящих в состав комплексов. [4]
Комплексный ион, образованный из простых, значительно больше их по размеру. Как следствие этого, меняется плотность заряда на поверхности и его свойства. Так, образование комплексных кислот из простых обычно сопровождается увеличением силы кислоты. Это объясняется тем, что энергия связи с ионами Н падает и сила кислоты соответственно растет. [5]
Комплексные ионы диссоциируют в растворе, как слабые электролиты - ступенчато, причем каждая ступень диссоциации может быть охарактеризована константами диссоциации, которые для комплексных соединений называют константами нестойкости. [6]
Комплексные ионы могут содержать во внутренней сфере в качестве аддендов молекулы аммиака или воды, или же анионы различных кислородных и бескислородных кислот. Если же аддендами являются анионы кислот, то получаются комплексные анионы, например [ Fe ( CN) 6 ] - , [ PtCle ] 2 -, [ Co ( NO2) 6 ] 3 - Эти соединения называют ацидокомплексами. Аци-докомплексы могут содержать в качестве комплексообразователя не только металлы, но также металлоиды, например мышьяк или сурьму, и неметаллы, например углерод, азот или серу. Эти кислотные радикалы ( анионы кислот) в свою очередь могут входить в качестве аддендов во внутреннюю сферу комплексных анионов. [7]
Комплексный ион [ Fe ( CN) e ] 4 - представляет собой соединение положительного иона Fe2 с шестью отрицательными ионами CN -; в других случаях вместо отрицательных ионов в состав комплексов могут входить нейтральные молекулы NH3, H2O и некоторых других веществ. [8]
Комплексные ионы [ Co ( SCN) 4 ] 2 - окрашены в синий цвет, а гидратированные ионы Со ( Н20) е ] 24 - в розовый. [9]
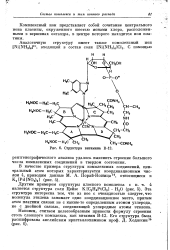 |
Структура витамина В-12. [10] |
Комплексный ион представляет собой сочетание центрального иона платины, окруженного шестью ионами хлора, расположенными в вершинах октаэдра, в центре которого находится ион платины. [11]
Комплексный ион не имеет идеальной симметрии Oh, a искажен так, что центр симметрии нарушен. [12]
Комплексные ионы обычно слабо диссоциируют, и поэтому реакция протекает практически необратимо в сторону их образования. [13]
Комплексный ион [ BF t ] - имеет тетраэдрическое строение, которое характерно и для других соединений бора, имеющих донорно-акцепторные 0-связи. В этих соединениях формируются 4 кова-лентные о-связи, образующиеся из хр3 - гибридных орбиталей атома бора. [14]
Комплексные ионы во многих случаях дают новые, совершенно другие характерные реакции. [15]
Страницы: 1 2 3 4