Малый ион
Cтраница 1
Малые ионы могут оказать существенное влияние на равновесие реакции образования комплекса. По мере диффузии низкомолекулярного электролита из зоны реакции степень превращения постепенно увеличивается, и в результате образуется комплекс, максимально удовлетворяющий условиям термодинамического равновесия. [1]
Малые ионы обладают подвижностью порядка I см. сек на 1 вся, большие ионы - 10 - 2 - 10 - см сек на 1 в. [3]
Связывание малых ионов полигонами в значительной степени определяет растворимость иолиэлектролитов в р-рах солей. [4]
Связывание малых ионов полиионами в значительной степени определяет растворимость полиэлектролитов в р-рах солей. [5]
Жесткость малым ионам придает только сольватация протонными растворителями ( симбиоз; см. разд. [6]
Применительно к малым ионам часто используют термин ионофорез, но это едва ли целесообразно, так как никаких принципиальных различий здесь нет. [7]
Следовательно, такие малые ионы, как Н, Li и Na, могут проникнуть в нормальные структурные пустоты воды и стабилизовать эту структуру, в то время как все большие ионы будут вызывать лишь ее разрушение. Подобный вывод представляется сомнительным, ибо ион F - и большинство многовалентных ионов в основном относятся к группе образовате-лей структуры. Трудно представить, что присутствие-этих ионов совместимо с существованием нормальной структуры воды. Тщательное исследование природы гидратации, как будет показано в дальнейшем, выявило полную несостоятельность модели Васлова. Наиболее вероятно, что истинная картина гидратированных ионов лежит между моделями Франка и Вена и Самойлова. [8]
Мембрана проницаема для малых ионов, и поэтому ионы хлора будут двигаться справа налево, так как ионы стремятся равномерно распределиться по всему объему. Каждый ион хлора, проходящий через мембрану, должен сопровождаться ионом натрия, иначе с внешней стороны мембраны накапливались бы положительные заряды. Пусть х означает концентрацию, которой достигли ионы хлора за время установления равновесия. Белок не может диффундировать через мембрану и остается с ее внутренней стороны. [9]
Мембрана проницаема для малых ионов, и поэтому ионы хлора будут двигаться справа налево, так как ионы стремятся равномерно распределиться по всему объему. Каждый ион хлора, проходящий через мембрану, должен сопровождаться ионом натрия, иначе с внешней стороны мембраны накапливались бы положительные заряды. Пусть к означает концентрацию, которой достигли ионы хлора за время установления равновесия. Белок не может диффундировать через мембрану и остается с ее внутренней стороны. [10]
Например, в иодидах малый ион лития настолько поляризует облако заряда иодид-иона, что возникает некоторая делокализация электронов; у ионов других щелочных металлов этот эффект значительно менее заметен. [11]
Закон, описывающий адсорбцию малых ионов в области концентрированных растворов низкомолекулярного электролита, свидетельствует о кооперативной адсорбции малых ионов. Это может быть следствием гетерогенной структуры гелей полиэлектролитного комплекса, состоящих из неупорядоченных областей, способных нормально адсорбировать низкомолекулярные электролиты, и упорядоченных ( лестничных) областей, способных поглощать малые ионы только в процессе кооперативной реакции обмена. Эти смолы представляют собой сшитый анионит, в клетках которого находится противоположно заряженный и взаимодействующий с ним слабый полиэлектролит. [12]
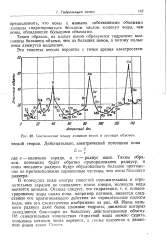 |
Соотношение между атомным весом и атомным объемом. ческой теории. Действительно, электрический потенциал иона. [13] |
Таким образом, из малых ионов образуются гидратные комплексы большего объема, чем из больших ионов, а потому малые ионы движутся медленнее. [14]
Дебая, определяемый концентрацией малых ионов M ( Na) в твердой фазе; V - парциальный моляльный объем электролита MX или НХ; и - давление контракции сшивания смолы; ам и ам - активности малых противо-ионов в растворе и в твердой фазе соответственно. В табл. 5 сведены результаты измерений. [15]
Страницы: 1 2 3 4