Малый ион
Cтраница 2
Обратимость четко проявляется при обмене малых ионов и для набухающих обменников. [16]
 |
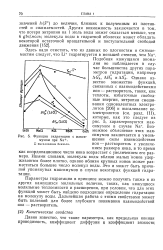
Зависимость сорбции ионов переходных металлов анионитами от ионной силы раствора р, ( См0 05 моль / л. [17] |
В этих условиях образуются ассоциаты малых ионов, степень гидролиза протонированных аминогрупп снижается и соответственно уменьшается координационная активность анионитов. [18]
Такие смолы пригодны для хроматографии малых ионов, а смолы с низкой степенью сшивки ( 2 - 4 %) применяют для хроматографии макромолекул. Обычно ионообменные смолы представляют собой микропористые сферические частицы диаметром менее 10 мкм, диаметр пор ( 1 5 - 10 мкм. Они обладают приемлемой эффективностью и высокой ионообменной емкостью. [19]
 |
Функции гидратации с максимумом при Na. [20] |
Иными словами, молекулы воды вблизи малых ионов удерживаются более плотно, однако вблизи крупных ионов может разместиться большее число молекул воды. Это и может быть причиной упомянутых максимумов в случае некоторых функций гидратации. [21]
Эта формула справедлива, если радиус малого иона не превышает 0.88 радиуса большого иона решетки. Если он превышает это значение, то раньше сам замещающий ион коснется одинаково заряженных ионов, чем ионы в сдвинутых им рядах - ионов соседних рядов. [22]
Значительные энергии гидратации, например Li ( очень малый ион по размеру) и Са2, объясняют тот факт, что элек-родные потенциалы этих металлов более отрицательны, чем у натрия, несмотря на то, что потенциалы ионизации у лития и кальция больше. [23]
Нитриты устойчивее HN02 ( в молекуле кислоты ничтожно малый ион Н, внедряясь в электронную оболочку атома О, ослабляет связь N-О), но только нитриты щелочных металлов плавятся без разложения. При термическом разложении нитритов образуется оксид металла. Нитриты, так же как и HNO2, обладают окислительной и восстановительной активностью. В растворах они постепенно окисляются, переходя в нитраты. [24]
Нитриты устойчивее HNO2 ( в молекуле кислоты ничтожно малый ион Н, внедряясь в электронную оболочку атома О, ослабляет связь N-О), но только нитриты щелочных металлов плавятся без разложения. Нитриты, так же как и HNO2, обладают окислительной и восстановительной активностью. В рас -, творах они постепенно окисляются, переходя в нитраты. [25]
Присутствие в составе стекла в качестве модификаторов малых ионов Zr4 и Mg2, стягивающих решетку, и крупных ионов Sr2, Ва2, Са2 обеспечивает высокую плотность фритты, которая необходима для затруднения диффузии серебра в резистивный слой из контактных площадок. В составе фритты не должно быть много ионов свинца, иначе их высокая подвижность при вжигании ( при 550 С) нарушает равновесность окислительно-восстановительны процессов, протекающих с серебряно-палладиевым наполнителем. В интервале температур 400 - 800 С стекло 279 - 2 инертно к Pd-A. Применение в качестве фритты боросвинцового стекла, например 660а, не отвечает приведенным выше условиям. [26]
Модель жесткого стержня позволяет оценить только распределение малых ионов относительно полииона. Она реальна для нек-рых биополимеров, напр, нативной ДНК или полипентидов в конформации а-спирали. [27]
Модель жесткого стержня позволяет оценить только распределение малых ионов относительно полииона. Она реальна для нек-рых биополимеров, напр, нативной ДНК или полипептидов в конформации ос-спирали. [28]
С увеличением ионной силы раствора возрастает концентрация малых ионов в фазе ионита, растет эффективность экранирования его ионизированных групп, что с избытком компенсирует незначительное уменьшение расстояния между ионогенными группами полимеров, вызванное его сжатием. Это определяет неоднозначное влияние ионной силы раствора на координационные свойства различных типов ионитов. Если координационно-активными являются ионизированные группы полимера ( например, катионитов), то с возрастанием ионной силы раствора показатели координационных свойств ионита уменьшаются, несмотря на некоторое увеличение их кислотности и снижение степени гидролиза ионизированных групп. Вероятно, это можно объяснить экранированием координационно-активных ионизированных групп полимера малыми ионами электролита и снижением степени набухания катионита. [29]
Уравнение ( 66) качественно выполняется для сравнительно малых ионов, которые требуют больших теплот выделения. Однако давно известно [51], что оно не дает количественного согласия с опытными данными. [30]
Страницы: 1 2 3 4