0-комплекс
Cтраница 2
Реакция азосочетания протекает через стадии образования - 0-комплекса и протолиза последнего. При этом активной формой аминосоединений в реакциях азосочетания является свободный ( неионизированный) амин. [16]
Важно также, чтобы винильная группа в исходном 0-комплексе непосредственно примыкала к атому металла, так как использование в реакции ( Т - циппамоильного производного III не привело к желаемому комплексу. В результате реакции был выделен комплекс IV, который при нагревании перешел в сг я-биядерный комплекс, но с элиминированием кетонной СО-группы. [17]
Это является следствием того, что в промежуточном 0-комплексе атом углерода, у которого идет замещение, приобретает тетраэдрическую конфигурацию, так как находится в р3 - гибридном состоянии, а атом брома оказывается выведенным из плоскости ароматического ядра. В конечном продукте после отрыва протона атом брома должен располагаться в этой плоскости, что приводит к значительному стерическому взаимодействию с объемистыми грег-бутильными группами. В результате отрыв протона идет медленно, и вторая стадия реакции становится скоростьопределяющей. [18]
Образование я-комплекса протекает быстрее, чем преаращение в 0-комплекс и обратное образование ароматического состояния. Какая из последних двух ступеней определяет скорость реакции, зависит от энергетического положения обоих переходных состояний. В последнем случае наблюдают кинетический изотопный эффект: соединения, в которых соответствующий атом водорода замещен атомом дейтерия или трития, реагируют медленнее. [19]
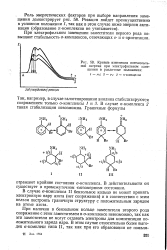 |
Кривые изменения потенциальной энергии при электрофильном замещении в различные положения. [20] |
При электрофильном замещении заместители первого рода повышают стабильность 0-комплексов, отвечающих о - и л-ориентации. [21]
Этот факт, по-видимому, объясняется большей стабильностью соответствующего промежуточного 0-комплекса ( биполярного иона) вследствие компенсации в нем положительного и отрицательного зарядов. [22]
Ароматические соединения также образуют л-комплексы в, переходящие в 0-комплексы с двух - или шеститочечной ориентацией. [23]
Предполагают, что метальные заместители кольца благодаря гиперконъюгации могут стабилизировать 0-комплекс. [24]
Ароматические соединения также образуют it - комплексы в, переходящие в 0-комплексы с двух - или шеститочечной ориентацией. [25]
Сульфирование и десульфирование проходят через промежуточное образование одного и того же 0-комплекса, который в первом случае образуется в результате присоединения к ароматическому соединению катиона HSO, а во втором - путем протонирования сульфокислоты. Обе рассматриваемые реакции - типичные реакции электрофильного замещения и поэтому подчиняются одним и тем же закономерностям. Чем легче идет реакция сульфирования, тем легче и десульфируется полученная сульфокислота. [26]
С точки зрения теории МО, основной причиной, определяющей низкую стабильность нестабилизированных 0-комплексов переходных металлов, является малая разница в энергиях высшей занятой d - орбитали металла и разрыхляющей а - молекулярной орбитали, связывающей металл с углеродом. Поэтому при незначительном возбуждении электронов металла они переходят на ст - разрыхляю-щую орбиталь и деформируют комплекс. При координации металла и электронодонорного органического лиганда возникают Дативные связи, благодаря которым разность энергий d - и сг - орбиталей увеличивается, а, следовательно, возрастает прочность комплекса. Такая координация снижает влияние и второй причины дестабилизации - перехода электронов с а-связывающей на вакантную rf - орбиталь, которая при взаимодействии, с электронодонорным лигандом оказывается заполненной. [27]
 |
Энергии орбиталей для взаимодействия нитрогруппы с пентадиенильным. [28] |
Высказано предположение [21], что если сопряжение между нитрогруппами и кольцом в циклогексадиенатном 0-комплексе близко к нулю, то я-электронная система представляет собой цепь с нечетным числом линейно связанных углеродных атомов, что приводит к несвязывающей орбитали грпь, обладающей большей энергией, чем у наивысшей незанятой МО в присоединенной нитро-группе или нитрогруппах ра. [29]
Как и другие реакции электрофильного ароматического замещения, бромирование протекает с промежуточным образованием катионных 0-комплексов. Симбатность между скоростями бр-омирования метилбензолов и устойчивостями а-комплек-сов ( но не л-комплексов) рассматривается как свидетельство - образования о-комплексов на лимитирующей стадии ( см. разд. Отсутствие изотопного эффекта водорода означает, что отрыв протона от о-комплекса с превращением в конечный продукт осуществляется быстро и не влияет на скорость всего процесса. [30]
Страницы: 1 2 3 4