Гидратированный ион - медь
Cтраница 1
Гидратированный ион меди () Си ( Н2О) 4 обладает светло-синей окраской, которая наблюдается в водных растворах солей меди ( II) и в некоторых кристаллогидратах. Металлическая медь не настолько активна, чтобы замещать ион водорода в разбавленных кислотах ( в ряду напряжений она занимает место ниже водорода; гл. [1]
Гидратированный ион меди ( П) Си ( Н20) обладает светло-синей окраской, которая наблюдается в водных растворах солей меди ( П) и в некоторых кристаллогидратах. Металлическая медь не настолько активна, чтобы замещать ион водорода в разбавленных кислотах ( в ряду напряжений она занимает место ниже водорода; гл. [2]
Гидратированные ионы меди имеют голу-бую окраску. [3]
Ионы хлора бесцветны, а гидратированные ионы меди имеют голубую окраску. Если же диссоциация неполная и часть молекул не распалась, раствор будет зеленым. Как известно, при смешивании голубой и желтой красок получается зеленая. [4]
Все рассматриваемые катионы бесцветны, за исключением гидратированного иона меди ( Си), сообщающего разбавленным водным растворам голубой цвет. [5]
Гидратированные ионы часто отличаются от негидратирован-ных даже по своим физическим признакам: например, ионы Си 1 1 белого цвета, тогда как гидратированные ионы меди [ Си ( ОН2) 41 имеют синий цвет; или другой пример: ионы Со темносинего цвета, а гидратированные ионы [ Со ( ОН2) 6 ] красного цвета. [6]
Действительно, было установлено, что при добавлении избытка гидроокиси аммония образуются новые ионные частицы темно-голубого цвета и они представляют собой медно-аммиачный комплекс Cu ( NH3) 4, аналогичный гидратированным ионам меди CuftbO) с той разницей, что четыре молекулы воды заменены молекулами аммиака. Этот комплекс называют тетрамминмедь ( II) - комплексом, при этом слово аммин означает присоединенную молекулу аммиака. [7]
В комплексе [ Cu ( NHs) 4 ] можно заместить NHs водой и получить комплекс [ Си ( ОНг) 4 ] н; последний представляет собой, вероятно, гидратированный ион меди. Аналогично этому комплекс [ Ni ( OH2) e ] H, который можно получить из соответствующего аммиачного комплекса, имеет строение гидратированного иона никеля. Гидратированные ионы, следовательно, являются комплексными ионами. [8]
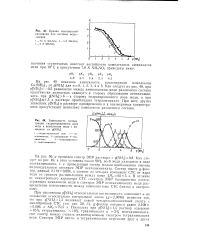 |
Кривая комплексооб-разования для системы медь -. шмиак.| Зависимость концентрации гидратированного иона меди и комплексов меди с аммиаком от pi [ NH3 ]. [9] |
Как следует из рис. 49, при р [ МНз ] - 0 5 равновесие между аммиакатами меди различного состава практически полностью сдвинуто в сторону образования пентааммиа-ката, при p [ NH3 ] 6 - в сторону гидратированного иона меди, а при p: [ NH3 ] l 5 в растворе преобладает тетрааммиакат. При всех других значениях p [ NH3 ] в растворе одновременно и в соизмеримых концентрациях присутствуют несколько комплексов различного состава. [10]
 |
Схема растворения кристалла NaCl в воде. Диполи - молекулы воды. Справа показано возникновение гидратных оболочек. [11] |
Гидратация иона Си2 в водных растворах происходит таким образом, что облака электронных пар четырех атомов кислорода, входящих в состав четырех, молекул воды, распределяются симметрично вокруг Си2, образуя плоскую фигуру. Гидратированный ион меди Си2 - 4Н2О придает раствору характерную голубую окраску. Изменение цвета в результате сольватации встречается довольно часто. [12]
Как и при анализе смеси катионов II и III аналитических групп, следует обратить внимание на окраску раствора. Вместе с окрашенными катионами III группы возможно присутствие в растворе гидратированных ионов меди [ Си ( Н2О) 4 ] 2, голубой цвет которых может быть маскирован ионами кобальта, хрома и некоторыми другими. [13]
Как и при анализе смеси катионов II и III аналитических групп, следует обратить внимание на окраску раствора. Вместе с окрашенными катионами III группы возможно присутствие в растворе гидратированных ионов меди [ Cu ( HzO) 4 ], голубой цвет которых может быть маскирован ионами кобальта, хрома и некоторыми другими. [14]
Никакой реакции не происходит: медь не вытесняет железа из его солей. Тотчас железо покрывается розовым слоем меди, а голубая окраска раствора, свойственная гидратированным ионам меди, постепенно исчезает, сменяясь зеленоватой окраской гидратированных ионов железа. Железо вытесняет медь из растворов ее солей. В растворе он полностью расщеплен на ионы меди и ионы кислотного остатка. [15]
Страницы: 1 2