Гидратированный ион - водород
Cтраница 2
Прежде чем перейти к рассмотрению того, что понимают химики под символом Н ( води) ( гидратированный ион водорода), мы должны более широко изучить взаимодействие ионов с водой. [16]
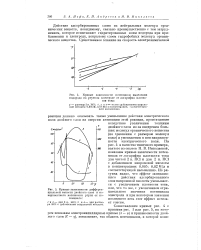
Действие адсорбированных слоев из нейтральных молекул органических веществ, повидимому, связано преимущественно с тем затруднением, которое испытывают гидратированные ионы водорода при приближении к электроду, покрытому слоем гидрофобных молекул органического вещества. [18]
Это объясняется тем, что по условиям электронейтральности через стеклянную мембрану из одного раствора в другой не могут проходить гидратированные ионы водорода ( Н3О) без какого-либо аниона. [19]
Особенности поведения стеклянного электрода как в неводных, так и в кислых водных растворах нельзя объяснить проникновением через стеклянную мембрану гидратированных ионов водорода, как это было принято Долом. [20]
Так как ионы Na tJlp и С1 др остаются в неизмененном виде, то теплота нейтрализации в этом случае отвечает реакции образования жидкой воды из гидратированных ионов водорода и гидроксила. [21]
В последнем варианте через катионитовую диафрагму МК-41 из анслита в католит ( в I секцию) переходили не ионы трехвалентного железа и других металлов, а гидратированные ионы водорода. [22]
В водных растворах реакция диссоциации сильных кислот протекает полностью независимо от того, существовал первоначально в молекуле кислоты ион водорода, который только подвергся гидратации, или же гидратированные ионы водорода образовались в растворе в результате реакции воды с атомами водорода, которые были связаны ковалентной связью. [23]
Например, под действием излучения происходит радиолиз водосодержащих сред и образование в них как долгоживущих продуктов типа перекиси водорода и молекулярного водорода, так и ряда короткоживущих продуктов типа свободных радикалов ( ОН), атомов и гидратированных ионов водорода. [24]
 |
Две возможные формы существования протона в воде, не считая Н3О. Существование обеих этих частиц установлено экспериментально. [25] |
Сказанное выше заставляет прийти к выводу, что для правильного описания протона в растворе недостаточно представления о какой-либо одной частице. Символически гидратированный ион водорода, т.е. протон, окруженный молекулами воды, обозначают как Н ( водн. [26]
 |
Прибор для получения и собирания. водорода и других газов. [27] |
Его получают непосредственно в растворах взаимодействием кислоты с металлами. В этом случае гидроксоний ( гидратированный ион водорода) восстанавливается до атомарного водорода. [28]
Реакция нейтрализации - это химическая реакция между веществом, имеющим свойства кислоты, и веществом, имеющим свойства основания, которая приводит к потере характерных свойств обоих соединений. Наиболее типичная реакция нейтрализации в водных растворах происходит между гидратированными ионами водорода и ионами гидро-ксила, содержащимися соответственно в сильных кислотах и основаниях: Н ОН-Н2О. [29]
Не подлежит сомнению, что на поверхности, полностью покрытой атомами водорода, разряд ионов может происходить только при юявлении просветов в адсорбционном слое или при выделении моле-улярного водорода без адсорбции атомов на поверхности. Энергия истивации, или энергетический барьер, который надлежит преодо-теть гидратированному иону водорода при непосредственном переходе молекулярному состоянию, должны быть гораздо выше, чем при лолизации после адсорбции. Действительно: во-первых, притяжение юна водорода к адсорбенту облегчает его дегидратацию при раз-эяде и превращении его в водородный атом; во-вторых, рекомби-иция атомов должна, как всегда, облегчаться твердой поверхностью. Это, повидимому, подтверждает правильность теории, согласно которой задержка происходит в процессе расчистки места в ад-горбционном слое на поверхности. [30]
Страницы: 1 2 3