Гидратированный ион - водород
Cтраница 3
Электролит представляет собой пластину толщиной 0 25 - 0 5 мм. В таком электролите отсутствуют свободные кислоты или основания; ионная проводимость обеспечивается лишь за счет подвижности гидратированных ионов водорода. Эти ионы движутся через слой электролита, переходят от одной сульфокислотной группы к другой, поэтому концентрация кислоты в электролите остается постоянной. Вода на аноде разлагается с образованием кислорода, ионов водорода и электронов. Ионы водорода диффундируют через твердый полимерный электролит и попадают на катод. Электроны проходят через внешний контур и достигают водородного электрода, где осуществляется рекомбинация водородных ионов и электронов с образованием молекул водорода. [31]
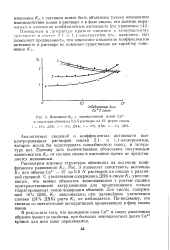 |
Изменение Кс с эквивалентной долей Са2 в смоле при обмене из 0 5 Л раствора на Н - фсрме смолы. - 24 % ДВЕ. 2 - 16 % ДВЕ. 3 - 10 % ДВБ. 4 - 2 % ДВБ. [32] |
Рассмотрим влияние структуры обменника на величину коэффициента равновесия Кс - 3 позволяет сопоставить величины Кс Для обмена Са2 - Н из 0 5 N растворов на смолах с различной сшивкой. С увеличением содержания ДВБ в смоле Кс увеличивается, что можно объяснить возникающими с ростом сшивки пространственными затруднениями для проникновения сильно гидратированных ионов водорода в обменник. Для смолы, содержащей 16 % ДВБ, К с максимальна; при дальнейшем увеличении сшивки ( 24 % ДВБ) роста Кс не наблюдается. По-видимому, это связано со значительной дегидратацией проникающих в фазу смолы ионов. [33]
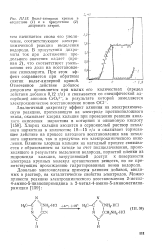 |
Вольт-амперные кривые в. [34] |
Хлорид кальция вводится в сернокислый раствор исходного наркотина в количестве 10 - 15 г / л и оказывает тормозящее действие на процесс катодного восстановления как исходного наркотина, так и продуктов его электрохимического окисления. Влияние хлорида кальция на катодный процесс связывается с образованием на катоде за счет подщелачивания, происходящего в результате выделения водорода, пористой пленки из гидроксида кальция, затрудняющей доступ к поверхности электрода крупных молекул органических веществ, но не препятствующих прохождению гидратированных ионов водорода. [35]
Вот почему для соляной кислоты при атмосферном давлении и температуре 25 С эта концентрация предельна. Сравнивая процессы (10.1) и (10.2), видим принципиальное различие между ними с точки зрения их осуществимости. Выгодность процесса (10.2) определяется экзоэргичностью образования гидратированных ионов водорода и хлора. [36]
Схема их проста ( рис. 180): к мембране с обеих сторон прижаты сетчатые или пористые электроды, покрытые слоем катализатора. Мембрана ( ка-тионообменная в Н - форме) с электродами зажимается между газовыми камерами, в которые подаются водород и кислород. Так как ток при этом переносится гидратированными ионами водорода, то вода образуется на положительном электроде. Она отводится от электродов током кислорода, от которого может быть отделена при проходе через конденсатор. Кроме того, она может быть отведена фитилями, прижатыми к задней стороне кислородного электрода, по которым вода под давлением газа выдавливается в водосборник сквозь войлочную прокладку, предохраняющую от выхода газа. [37]
Очевидно, что т является суммарным временем, необходимым как для диффузии электролита через толщу пленки, так и для накопления кислоты за пленкой в количестве, достаточном для изменения цвета индикатора. Вследствие этого при использовании указанной методики концентрационная зависимость D искажается концентрационной зависимостью проницаемости. Авторы объясняют найденную концентрационную зависимость D следующим образом: размер диффундирующей пары гидратированный ион водорода анион кислоты значительно больше недиссоциированной молекулы кислоты, поэтому последняя диффундирует с большей скоростью, а так как с увеличением концентрации кислоты возрастает доля недиссоциированных молекул, то это приводит к росту D с концентрацией раствора. Иными словами, авторы предполагают, что перенос кислот через пленки осуществляется частицами различной природы и размера. [38]
Ионно-электростатическая компонента расклинивающего давления, согласно [42, 45], зависит, главным образом, от потенциалов поверхностей, ограничивающих пленку. Поскольку изученные нами ПАВ являлись неионогенными и при их добавлении ионная сила дисперсионных сред оставалась постоянной, а концентрации ионов в отсутствие NaCl при рН 6 - - 7 были достаточно низки, в первом приближении можно полагать равенство электрокинетических и штерновских потенциалов. Следовательно, обнаруживаемое в опыте повышение - потенциала при увеличении содержания ПАВ в интервале от Ы0 - 7 до 1 - 10 - 5 - 1 - 10 - 4 моль / дм3 ( рис. 12.5) обусловлено вытеснением из слоя Штерна сильно гидратированных ионов водорода. [39]
Ни то, ни другое предположение экспериментально не подтверждено. Большинство других ионов также образуют гидраты переменного состава. Поэтому лучше не изображать ион водорода как Н3О, или Н9О, или Н7О3, а изображать как Н ( води), что означает гидратированный ион водорода. Аналогично следует поступать и при написании других гидра-тированных ионов. [40]
ГИДРОКСЙДЫ ПРИРОДНЫЕ, подкласс ( или класс) минералов, природные вод. оксиды металлов. Неограниченно растворим в воде. Взаимодействуя с к-тами, образует соли, напр. Применяют в произ-ве капролактама, в аналитич. ГЙДРОКСОНИЙ, НзО, гидратированный ион водорода; существует в вод. р-рах кислот. [41]
ГИДРОКСЙДЫ ПРИРОДНЫЕ, подкласс ( или класс) минералов, природные вод. оксиды металлов. Неограниченно растворим в воде. Взаимодействуя с к-тами, образует соли, напр. Применяют в произ-ае капролактама, в аналитич. ГИДРОКСОНИЙ, НдО, гидратированный ион водорода; существует в вод. р-рах кислот. [42]
В карбонильной группе электроны смещаются от атома углерода к кислороду как более электроотрицательному элементу. В результате этого углерод проявляет некоторый положительный заряд и притягивает к себе электроны от второго атома кислорода из гидроксильной группы. Тогда связь между кислородом и водородом гидроксильной группы сильно ослабляется и становится возможным отщепление водорода. Карбоновые кислоты, подобно минеральным, образуют в водных растворах гидратированные ионы водорода. [43]
Для объяснения закономерностей ионообменных процессов был выдвинут ряд теорий; наиболее обещающими из современных теорий являются представления Грегора. Согласно его теории, ионообменную смолу следует рассматривать как набухший гель, в котором установилось равновесие между давлением набухания ( или осмотическим давлением) и упругими силами сшитой матрицы полимера. Всякое изменение условий нарушает этот баланс, и система переходит в новое состояние равновесия. Так, например, если полностью набухшую смолу в натриевой форме перевести в водородную форму, зерна ионита несколько увеличатся в размере; это увеличение тем меньше, чем больше степень поперечной сшивки смолы. В результате устанавливается новое равновесное состояние, при котором приращение объема ионита будет меньше, чем разница объемов гидратированных ионов водорода и натрия. С уменьшением степени сшивки уменьшаются и силы упругости, возникающие при данном приращении объема, в связи с чем количество свободной воды, выжимаемой из матрицы ионита при заданном изменении ионного состава, будет меньше, а конечное увеличение объема смолы, следовательно, будет больше. [44]
Страницы: 1 2 3