Сферический ион
Cтраница 1
Очень большие сферические ионы почти не сольватируются из-за, малой плотности зарядов на их поверхности, и величины радиусов этих ионе. [1]
Очень большие сферические ионы почти не сольватируготся из-за малой плотности зарядов на их поверхности, т величины радиусов этих ионов не зависят от природы растворителя. [2]
Рассмотрим сферический ион радиуса Ь, находящийся в среде, состоящей из двух смешивающихся неэлектролитов. [3]
Модель сферических ионов является грубым приближением. Это видно, например, при расчете с ее помощью дипольных моментов молекул. [4]
Рассмотренная модель сферических ионов позволяет выполнять расчеты и других молекулярных параметров помимо энергии диссоциации, например дипольного момента. Небольшие расхождения с опытом объясняются несовершенством модели. [5]
 |
Термохимические циклы для расчета. [6] |
Говоря о сферических ионах, часто используют понятие радиус иона. Надо четко представлять себе, что скрывается за этим понятием. Как и в любом атоме, плотность электронного облака иона спадает до нуля только на бесконечности, хотя практически уже на расстоянии 3 - 5 - КГ 10 м ( 3 - 5 А) она неотличима от нуля. Поэтому строго определенного радиуса у иона, как и у атома, нет и быть не может, и, естественно, эта величина физическими опытами не может быть установлена. Радиус иона - понятие условное, но удобное в ряде случаев. На опыте измеряется межъядерное расстояние. [7]
Согласно представлениям о сферических ионах, следует эту решетку представить себе, составленной из соприкасающихся между собою шаров. [8]
 |
Ион белка с дискретными зарядами. Точки k и / изображают положения двух зарядов. [9] |
Как и в случае сферических ионов, уравнения этого раздела неприменимы ни для сильно концентрированных растворов, ни для растворов, не содержащих добавленного электролита. [10]
Считается, что справедливо предположение о несжимаемых сферических ионах и обязательно требование контакта между катионом и окружающими его анионами. Иначе говоря, катионы не должны болтаться в пустотах, которые образованы соприкасающимися друг с другом анионами. Каждый катион должен касаться по возможности большего числа анионов. [11]
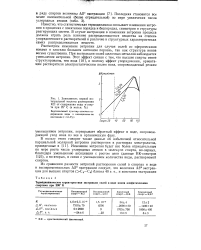 |
Зависимость первой интегральной теплоты растворения КС1 от содержания воды в спирте при 25 С ( в мольн. %. [12] |
Рассмотрим изменение энтропии для случая солей со сферическими ионами и плоским большим катионом порознь, так как структура ионов весьма существенна. При экстракции солей щелочных металлов наблюдается уменьшение энтропии. [13]
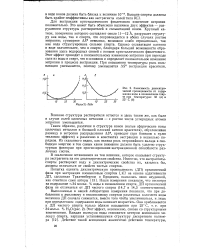 |
Зависимость диэлектрической проницаемости от содержания воды в изоамиловом спирте при температурах 50 ( а и 25 С ( б. [14] |
Таким образом, различие в структуре ионов ( малые сферические ионы щелочных металлов и большой плоский катион красителя), обусловливая разницу в энтропии распределения AS0, приводит ( при близком к нулю тепловом эффекте) к различию в константах экстракции в несколько порядков. Из сказанного видно, как велика роль энтропийного вклада в свободную энергию и тем самым какое внимание должно быть уделено структурным факторам при прогнозировании экстракционной способности различных систем. [15]
Страницы: 1 2 3 4