Сферический ион
Cтраница 3
В результате ион-дипольного взаимодействия свободные ионы, образующиеся из ионных пар, поляризуют вокруг себя молекулы растворителя. Картина ориентации диполей среды вокруг сферических ионов одинакова по всем направлениям. [31]
Как известно, в состоянии устойчивого равновесия система обладает минимумом потенциальной энергии. Энергия системы, состоящей из сферических ионов противоположного знака, будет, очевидно, уменьшаться при максимальном сближении ионов противоположного знака, но будет увеличиваться от сближения ионов одинакового знака. Поэтому при образовании ионных кристаллов обычно ближайшими соседями являются ионы с противоположными знаками, причем ионы противоположного знака должны соприкасаться. [32]
В высокотемпературной модификации КОН ионы ОН ведут себя как сферические ионы с эффективным радиусом 1 53 А, промежуточным между радиусами F - и С1 -; это соединение имеет структуру NaCl. Пока не установлено, является ли кубическая симметрия следствием случайной ориентации анионов или же результатом их свободного вращения. [33]
Так как ионы, имеющие электронную структуру благородных газов, сферически симметричны, они притягиваются к ионам противоположного знака в одинаковой степени в любом направлении. Простое электростатическое рассмотрение показывает, что ионная структура, содержащая сферические ионы А и В -, будет наиболее устойчива, если ионы касаются друг друга и расположены симметричным образом. Строение ионных соединений отгределяется двумя факторами: относительными размерами ионов и требованием электрической нейтральности структуры как целого. Размер ионов в основном определяет геометрию структуры; ее можно обсуждать, используя понятие координационных чисел. Наиболее устойчивой конфигурацией для координационного числа 2 является линейная В-А - В, так как для нее отталкивание между отрицательно заряженными ионами В - минимально; устойчивыми конфигурациями для координационных чисел 3, 4, 6 и 8 являются соответственно копланарная, тетраэдрическая, октаэдрическая и кубическая. [34]
Из этих уравнений виден характер зависимости менения свободной энергии, энтропии и энтальпии обменной реакции ( 1) от диэлектрической проницаемости, обеих фаз, температурных коэффициентов диэлектрической проницаемости, радиусов обменивающихся анионов и радиуса катиона четвертичного аммония. Без, сомнения, это упрощенная модель, в которой предполагаются сферические ионы в континууме и пренебре-гаются некоторые существенные факторы. Однако сопоставление результатов, полученных с помощью модели, с экспериментальными может пролить: свет на природу других факторов, действующих в процессе распределения. [35]
Поэтому эти два электрона аномально мало экранируют положительно заряженное ядро металла от отрицательно заряженных лигандов по сравнению с тем, что можно было бы ожидать при их сферически симметричном распределении в пространстве, и атомы лигандов приближаются к иону на более короткие расстояния. Поэтому в действительности радиус иона металла оказывается меньше, чем для гипотетического изоэлектронного сферического иона. Дают значительно меньший вклад в экранирование металла, чем можно было бы ожидать для трех d - электронов, распределенных по сфере. Однако для Сг2 и Мп2 мы имеем конфигурации tjbeg и t ge, в которых электроны, добавившиеся к конфигурации tjg в ионе V24 -, заняли орбитали, концентрирующиеся в основном между ионом металла, и лигандами. Электроны на е - орбиталях вносят в экранирование больший вклад, чем можно было бы ожидать для сферически симметричного их распределения в пространстве. И действительно, эффект настолько значителен, что происходит возрастание ионного радиуса. Та же последовательность событий повторяется во второй половине ряда. Три первых электрона, добавляющиеся к сферически симметричной t & - конфигурации Мп2, заполняют g - орбитали, их вклад в экранирование аномально мал, и радиусы поэтому уменьшаются аномально быстро. При переходе от Ni2 с конфигурацией t g к Си2 и Zn2 электроны заполняют g - орбитали, где их экранирующая способность аномально велика. Поэтому радиусы перестают уменьшаться, а в действительности даже обнаруживают некоторое увеличение. Аналогичные эффекты найдены для трехвалентных ионов, ионов металлов других переходных рядов и для тетраэдрических комплексов. [36]
В продукте дегидратации гексагидрата хлорида кобальта ( II) релаксация решетки наиболее велика. Поскольку продукты дегидратации алюмо-калиевых квасцов имеют открытую структуру, то здесь подвижность сферических ионов, образующих решетку, значительна в присутствии паров воды, а степень рекристаллизации оказывается большой. [37]
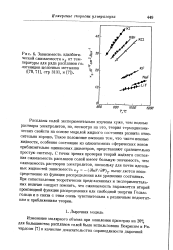 |
Зависимость адиабатической сжимаемости KS от температуры для ряда расплавов га-логенидов щелочных металлов (, стр 3131, и. [38] |
Расплавы солей экспериментально изучены хуже, чем водные растворы электролитов, но, несмотря на это, теория термодинамических свойств на основе моделей жидкого состояния развита относительно хорошо. Такое положение вызвано тем, что чисто ионные жидкости, особенно состоящие из одноатомных сферических ионов приблизительно одинаковых диаметров, представляют сравнительно простую систему. С точки зрения проверки теорий жидкого состояния сжимаемость расплавов солей имеет большую значимость, чем сжимаемость растворов электролитов, поскольку для почти идеальных жидкостей зависимость KT - ( d nV / dP) T вычисляется непосредственно из функции распределения или уравнения состояния. При сопоставлении теоретически предсказанных и экспериментальных величин следует помнить, что сжимаемость выражается второй производной функции распределения или свободной энергии Гельм-гольца и в связи с этим очень чувствительна к различным недостаткам и приближениям теории. [39]
 |
Первые потенциалы. [40] |
Электростатические силы притяжения между ионами Ме и Х - не приводят к их слиянию, как было бы, будь ионы точечными зарядами. Баланс сил притяжения и отталкивания определяет равновесное расстояние ге, на котором находятся центры сферических ионов в молекуле, и которому отвечает минимальное значение ее энергии. [41]
Этот термин впервые был предложен А. Ф. Капустинским ( 1934); он представляет собой эффективный радиус сферического иона, изоэнергетически замещающий данный ион в кристаллической решетке соли. Термохимические радиусы многих комплексных частиц были получены К. Б. Ядимирским, который широко использовал их для характеристики комплексных соединений. Следует отметить, что термохимический радиус несферической комплексной частицы не равен ни максимальному расстоянию от центра до его поверхности ( радиусу описанной сферы), ни минимальному расстоянию, а представляет собой некоторое среднее значение между этими двумя величинами. Колебания в этих величинах не превышают колебаний в величинах кристаллохимических радиусов ионов. [42]
Часто форма ионов сильно отличается от сферической, и поскольку ионы имеют величину того же порядка, что и молекулы растворителя, то вряд ли можно точно описать тормозящее влияние последних с помощью представления о макроскопической вязкости. В первом приближении можно считать, что условия применимости уравнения ( 1) соблюдаются для больших сферических ионов. Сочетая это уравнение с уравнением ( 15) гл. [43]
Ниже будет показано, однако, что сходство между гидроокисями и галоидопроизводными ограничено и что имеются значительные расхождения между структурами соединений этих двух рядов. Типичными различиями являются следующие: КС1 обладает простой ионной структурой каменной соли, которую и следует ожидать для сферических ионов, а КОН и KSH имеют эту структуру только при высоких температурах. Структура КОН при обычных температурах неизвестна, а менее симметричная структура низкотемпературной модификации KSH будет описана ниже. Упаковка групп ОН в некоторых гидроокисях металлов со слоистой решеткой значительно отличается от упаковки атомов галоида в солях галоидоводорпдных кислот, имеющих близкую формулу, что дает основание предполагать наличие направленных сил между соседними группами ОН, связанными с различными атомами металла. Подобные различия существуют между оксигндроокисями МО - ОН и оксихлоридами МО-С1. [44]
Ион SH - имеет приблизительно такой же размер, как Вг -, и является изоэлектрпн-ным с ионом С1 -, Таким образом, следует ожидать, что гидроокиси и гидросульфиды имеют структуры, подобные структурам галоидо-производных, и действительно, эти соединения имеют много общих свойств. В предыдущей главе мы видели, что в некоторых галогенидах ( например, в галогенидах щелочных металлов) галоид ведет себя как сферический ион; в других соединениях связи R - X имеют более ковалентный характер и образуются различные типы слоистых решеток. [45]
Страницы: 1 2 3 4