Неметаллический ион
Cтраница 1
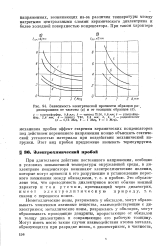 |
Зависимость электрической прочности образцов ра -. диокерамики от частоты ( а и от толщины образцов ( б. [1] |
Неметаллические ионы, разряжаясь у обкладок, могут образовывать химически активные вещества, взаимодействующие с диэлектриком; металлические ионы, разряжаясь у обкладок, могут образовывать проводящие дендриты, прорастающие от обкладок в толщу диэлектрика и сокращающие его рабочую толщину. [2]
Спектры неметаллических ионов в расплавленных солях систематически не исследовались, однако спектр МО. Особый интерес к спектрам поглощения расплавленных нитратов обусловлен тем, что положение максимума полосы минимальной энергии весьма регулярным образом зависит от катионного состава и температуры соли. Несмотря на то что это явление обсуждалось довольно широко, убедительная теория его еще не создана. Создание теории этого эффекта, вероятно, позволит в дальнейшем непосредственно изучать межмолекулярные взаимодействия. [3]
В наших расчетах электронной зонной структуры мы считали, что каждое занятое состояние является атомным электронным состоянием неметаллического иона. При этом, однако, имеются отличные от нуля матричные элементы между волновыми функциями каждого такого состояния и волновыми функциями пустых состояний соседних ионов. Это меняет волновые функции занятых состояний. [4]
Солевой раствор окружен мембранами, электрическое поле заставляет катионы ( металлы) мигрировать по направлению к катоду, а анионы ( неметаллические ионы) - мигрировать к аноду, таким образом обессоливая раствор. К сожалению, осуществление на практике этого процесса не так просто. Для процессов обессоливания энергия электродиализа должна также преодолевать осмотическое давление, проталкивающее чистую воду обратно в раствор. [5]
Металлические ионы, разряжаясь у обкладок, создают проводящие мостики, которые прорастают в глубь диэлектрика и приводят к уменьшению его толщины, а следовательно, и к снижению электрической прочности. Неметаллические ионы, разряжаясь у обкладок, могут образовывать химически активные вещества, разрушающие диэлектрик и снижающие его электрическую прочность. Указанные электрохимические процессы особенно резко проявляются при повышенных температурах. [6]
Маделунга почти компенсирует затраты энергии на ионизацию. В соединениях, состоящих из катионов, подобных инертному газу, положительные дырки локализуются на неметаллических ионах. Например, е - f - О3 - - О - ( или О2 - - О - И - О - В этом случае-энергия частичной рекомбинации - превышает потери локальной энергии Маделунга. [7]
Однако, как недавно отметил Пантелидес [49], такое представление не согласуется с утверждением, что основной пик в спектрах оптического поглощения соответствует переходу из состояний валентной зоны, сосредоточенных вблизи неметаллического иона, в состояние зоны проводимости, сосредоточенное на ионе металла. Напомним, что в разд, 4Л одна и та же сила осцилляторов определяла и интенсивность оптического поглощения, и диэлектрическую восприимчивость. [8]
Электрохимические процессы связаны с переносом ионов в диэлектрике, которые образуют ток утечки. Металлические ионы, разряжаясь у обкладок, образуют проводящие мостики, которые прорастают в глубь диэлектрика и приводят к уменьшению его толщины, а следовательно, и к снижению электрической прочности. Неметаллические ионы, разряжаясь у обкладок, могут образовывать химически активные вещества, разрушающие диэлектрик и тоже снижающие его электрическую прочность. Указанные электрохимические процессы особенно резко проявляются при повышенных температурах. [9]
Для ионных кристаллов координационное число определяется соотношением радиусов металлического и неметаллического ионов, так как каждый ион стремится притянуть к себе как можно больше ионов противоположного знака. В решетке ионы укладываются как шары разных диаметров. Радиус неметаллического иона больше радиуса металлического, и поэтому металлические ионы заполняют поры в кристаллической решетке, образованной ионами неметалла. В ионных кристаллах координационное число определяет число ионов противоположного знака, которые окружают данный ион. [10]
Френкель и Гейзенберг выдвинули предположение, что ферромагнетизм вызывается электрическим обменным взаимодействием между электронами, локализованными на соседних атомах кристаллической решетки, так называемым прямым обменом. При этом постулировалось, что по порядку величины интегралы прямого обмена не отличаются от соответствующих интегралов для молекулы водорода и могут быть положительными. В последующих работах в качестве причины ферромагнетизма кроме прямого обмена рассмотрены также обменные взаимодействия другого типа, например обменное взаимодействие между электронами, участвующими в переносе заряда, между почти свободными и связанными электронами ( s - d - и s - if - обмен) [5] и косвенный обмен через электроны неметаллических ионов в соединениях. [11]
К ним относятся сульфиды и оксиды. В таких соединениях преобладает ионный тип связи, и они имеют переменный состав. Избыток ионов металла в соединении создает электронную проводимость. При избытке неметаллических ионов соединение приобретает дырочную проводимость. [12]
Йодистая медь при высоких температурах ведет себя как материал с суперионной проводимостью. При низких температурах йодистая медь имеет структуру цинковой обманки, причем атомы иода расположены в узлах гранецентриро-ванной кубической решетки, а маленькие атомы меди находятся между ними в тетраэдрическом окружении. Это соединение имеет большую степень ионности, и изменение энергии было бы совсем невелико, если бы атомы меди лежали в октаэдрических положениях и кристалл имел бы симметрию каменной соли. При повышении температуры происходит превращение, при котором подрешетка. Очень часто подрешетка из неметаллических ионов меняет свою структуру при таком плавлении металлической подрешетки. Как в Agl, так и в СиВг при 146 и 485 С соответственно неметаллические ионы перестраиваются в объемоцентрированную кубическую решетку. При этом подрешетка из ионов благородного металла плавится. [13]
У нашей упрощенной теории с ее простыми расчетами имеется и еще одно затруднение. Так как взаимодействие из-за перекрытия волновых функций быстра спадает с расстоянием, то это утверждение оказывается верным, только если считать, что ионы обоих типов имеют приблизительно одинаковые размеры. На самом деле, если мы будем оценивать размеры ионов по размерам соответствующих атомов инертных газов, то простое геометрическое рассмотрение покажет, что в ионных кристаллах постоянная всегда определяется взаимодействием ближайших соседей. Однако если считать, что образование ионов сопровождается переносом протона, то ме таллический ион оказывается меньше, а неметаллический - - больше. Тогда постоянная решетки может определяться в основном взаимодействием неметаллических ионов, а металлические ионы при этом болтаются где-то между ними. Представление о том, что взаимодействие ионов хлор а определяет постоянную решетки, также использовалось для объяснения различных структур соединений галогенидов щелочных металлов. Например, было предположено, что ион цезия имеет размер, сравнимый с размером иона хлора. При этом постоянная решетки определяется суммой ионных радиусов цезия и хлора в обеих обсуждаемых структурах. Большая величина постоянной Маделунга для структуры CsCl делает реально существующей именно эту структуру. Ионы других щелочных металлов значительно меньше иона хлора, при этом постоянная решетки определяется взаимодействием ионов хлора. [14]
 |
Реакция дезаминирования цеолитов. [15] |
Страницы: 1 2