Однозарядный положительный ион
Cтраница 2
Атомы рубидия не образуют отрицательных ионов, но легко переходят в однозарядные положительные ионы. [16]
При адсорбции бария на вольфраме некоторое его количество существует на поверхности в виде однозарядных положительных ионов с радиусом около 1 8 10 8 см. Если концентрация адсорбированного бария мала, каждый его атом ионизирован. С ростом ч доля ионизированных атомов уменьшается. Когда к поверхности прикладываются большие положительные поля, ионы бария оттягиваются дальше от поверхности. Это приводит к уменьшению силы притяжения между ионами и зарядами их электрического изображения. При некоторой критической величине приложенного поля сила, стремящаяся оторвать ион от поверхности, слегка превышает силу притяжения иона и он десорбируется. С увеличением температуры среднее расстояние иона от поверхности возрастает и потому критическая величина поля уменьшается. [17]
Прежде чем рассматривать влияние добавления электрона к молекуле, удалим один электрон с образованием однозарядного положительного иона. Рассмотрим ион только в основном состоянии, как правило, соответствующем удалению одного электрона с ВЗМО молекулы. Этот процесс можно тщательно исследовать с помощью фотоэлектронной спектроскопии. Причина этого показана на рис. 12, изображающем поверхность потенциальной энергии для молекулы и иона в их основных состояниях. Ординатой является одна из нормальных координат молекулы, которая может иметь весьма отличающееся равновесное значение в ионе. [18]
При диссоциации атом натрия отдает атому хлора единственный электрон своей внешней оболочки и в результате становится однозарядным положительным ионом. Атом хлора имеет незаполненную внешнюю оболочку с семью электронами. Для заполнения этой оболочке недостает одного электрона, который она принимает от атома натрия и становится заполненной. Нейтральный атом хлора становится однозарядным отрицательным ионом. [19]
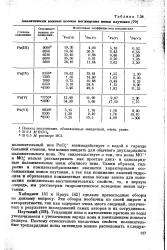 |
Аналитически важные полосы поглощения ионов плутония. [20] |
Это свидетельствует о том, что ионы МО и МО нельзя рассматривать как простые двух - и однозарядные положительные ионы обычного типа. Таким образом, гидролиз и комплексообразование являются характерными особенностями ионов плутония, а так как понимание явлений гидролиза и образования комплексных ионов весьма важно для понимания окислительно-восстановительных свойств, то, в первую очередь, мы рассмотрим гидролитическое поведение ионов плутония. [21]
Бомбардировка электронами может приводить к возникновению отрицательных ионов или многозарядных катионов, но гораздо более вероятным является образование однозарядных положительных ионов. В соответствии с этим в обычной масс-спектрометрии бомбардировка образца вызывает образование набора катионов за счет либо первоначальной ионизации, либо фрагментации, и эти ионы ускоряются в электрическом поле и отклоняются в магнитном. Принцип работы масс-спектрометра состоит в том, что пучок ионов с изменяющейся массой попадает в постоянное поле с изменяющимся потенциалом V или в изменяющееся поле с постоянным потенциалом, причем ионы разделяются по массам и их присутствие может быть зафиксирована при прохождении через очень узкую щель в виде узких пучков ионов с различными массами. Это не означает, что ионы с высоким молекулярным весом могут быть разделены с помощью этих приборов. [22]
В табл. V, 1 приведены в качестве примера значения функции ( Н т - Яо) / Т однозарядных положительных ионов некоторых элементов при температурах до 50000 К. При обычных температурах теплоемкость и внутренняя энергия одноатомных частиц не имеют колебательных и вращательных составляющих, а определяются всецело поступательным движением частиц. При - высоких же температурах еще прибавляется и энергия возбуждения более высоких энергетических уровней электронов. Переход от атомов Не к Ne, Аг, Кг, Хе и Rn сопровождается понижением первого уровня электронных возбуждений. Для ионов Li не обнаруживается возбужденных состояний еще при 45 000 К, для ионов Na - при 20000 К, для К и Rb - при 10000 К и для Св при 9000 К. Для изоэлектронных частиц чем выше заряд ядра, тем выше первый уровень электронных возбуждений и, следовательно, выше температура, при которой эти возбуждения начинают влиять на термодинамические функции. [23]
Склонность к переходу в одновалентное состояние убывает в ряду Т1 In Ga А1, и химия таллия - это в основном химия однозарядного положительного иона. Ион Т1 очень похож на ионы щелочных металлов тем, что он дает растворимые окись, карбонат, цианид и гидроокись. Нитрат, сульфат и перхлорат изоморфны с соответствующими солями калия. Однако бромат, иодат, сульфид и галогениды закисного таллия ( за исключением фторида) плохо растворимы в воде. Такое поведение сходно скорее с поведением солей Ag, чем солей щелочных металлов. [24]
Имеются также убедительные данные, что в кристалле любого щелочного металла на каждый атом приходится всего один делокализованный электрон, и этой конденсированной фазе присущи многие свойства, которые следует ожидать в системе из однозарядных положительных ионов, окруженных численно равным количеством электронов, образующих электронный газ. Например, при последовательном переходе от лития к цезию температуры кипения и плавления, а также твердость щелочных металлов уменьшаются вполне закономерно. Это согласуется с представлением о том, что размер положительного иона существенно определяет силы, удерживающие конденсированную фазу как единое целое. Маленькие ионы лития должны сильнее нритяливать окружающие электроны, чем более крупные ионы натрия, и эта закономерность выполняется при последовательном переходе к более тяжелым щелочным металлам по мере возрастания ионных радиусов. При этом возникает интересный вопрос: как один атом может координироваться восемью другими атомами, если на каждый атом приходится только один электрон, участвующий в связи. Интересно также выяснить, почему координационное число равно именно восьми. Почему оно не равно, например, двенадцати, как это обнаруживается в большинстве металлов. Ведь двенадцать - это максимальное число сфер, которые могут плотно упаковываться вокруг сферы такого же размера, если между ними не действуют какие-либо направленные силы. [25]
Нейтральные атомы щелочных металлов не обладают свойством принимать дополнительные электроны; наоборот, каждый из этих атомов удерживает очень слабо один из своих электронов, настолько слабо, что в присутствии галогена, который может принять электрон, такой атом щелочного металла теряет электрон, образуя однозарядный положительный ион. Катионы щелочных металлов, присутствующие почти во всех соединениях этих металлов, называются Li ионом лития, Na ионом натрия, К ионом калия, Rb ионом рубидия и Cs ионом цезия. [26]
 |
К задаче 10.| К задаче 15. [27] |
За каждую секунду нить испускает 3 - 1018 электронов, которые пересекают данную плоскость, двигаясь к аноду. Через ту же поверхность проходят также 0 6 - 10 однозарядных положительных ионов в обратном направлении. [28]
В системе могут образовываться новые электрически заряженные частицы, например электроны вследствие ионизации атомов и молекул, ионы за счет явления ионизации или электролитической диссоциации и др. Однако при этом одновременно рождаются частицы, заряды которых противоположны по знаку и в сумме равны нулю. Например, при ионизации атома образуется пара частиц - свободный электрон и однозарядный положительный ион. [29]
Процессы, приводящие к образованию положительно заряженного иона водорода, представляют особый интерес ( разд. Для осуществления этого процесса необходима значительно большая энергия, чем для образования других однозарядных положительных ионов, например ионов щелочных металлов. Те соединения, в которых атом водорода имеет хотя бы небольшой положительный заряд ( при электролизе водород выделяется на катоде), ведут себя в определенных растворителях как протонные кислоты. При этом образуются сольватирован-ные ионы водорода. Состояние протона в воде подробно рассмотрено в разд. [30]
Страницы: 1 2 3 4