Нитратный ион
Cтраница 3
 |
Классификация анионов по окислительно-восстановительным свойствам. [31] |
Обычно групповым реактивом на ионы-окислители рекомендуется брать другие вещества ( KJ или МпС12 НС1), но так как из ионов окислителей в настоящем руководстве рассматривается только нитратный ион, то можно взять в качестве группового реактива любой характерный восстановитель. [32]
Катионит служит также для удаления элементарного хлора. Затем нитратные ионы восстанавливаются до нитритных и определяются колориметрически. [33]
При экстракции технеция пиридином из такого раствора величина коэффициента распределения технеция составляет 740, тогда как большинство примесей пиридином практически не извлекается. Наличие нитратных ионов несколько снижает коэффициент распределения технеция, но все же он остается достаточно высоким. После экстракции пиридин отгоняют с водяным паром, в водном растворе вновь создается i концентрация 0 25 М NaOH и 2М Ма2СОз, и проводят повторную экстракцию технеция. Эта схема, по-видимому, может быть признана в настоящее время наиболее удачной, хотя 1наряду с нею предложено несколько других методов получения технеция из растворов отходов процессов переработки ядерного топлива. [34]
При экстракции технеция пиридином из такого раствора величина коэффициента распределения технеция составляет 740, тогда как большинство примесей пиридином практически не извлекается. Наличие нитратных ионов несколько снижает коэффициент распределения технеция, но все же он остается достаточно высоким. После экстракции пиридин отгоняют с водяным паром, в водном растворе вновь создается i концентрация 0 25 М NaOH и 2 М Na2CO3, и проводят повторную экстракцию технеция. Эта схема, по-видимому, может быть признана в настоящее время наиболее удачной, хотя наряду с нею предложено несколько других методов получения технеция из растворов отходов процессов переработки ядерного топлива. [35]
При суммарном определении низшие окислы i в HNOs; последняя в щелочном растворе дает с сульфофеноловой кислотой желтое окрашивание. Раздельное определение нитритных и нитратных ионов в разных частях одной пробы предложено Гуревичем [182], полярографический метод - Коганом. [36]
При суммарном определении низшие окислы окисляются в HNOs; последняя в щелочном растворе дает с сульфофеноловой кислотой желтое окрашивание. Раздельное определение нитритных и нитратных ионов в разных частях одной пробы предложено Гуревичем 182 ], полярографический метод - Коганом. [37]
Процессом окисления нитратных ионов может быть как окисление их самих, так и окисление гидратирующих их молекул воды. Продуктом того и другого окисления нитратных ионов являются, вероятно, молекулы кислорода. [38]
Примерами антагонистических отношений между ионами может служить подавление поступления нитратного иона при высокой концентрации фосфатного иона, и наоборот, и подобные же отношения между ионами калия и натрия, калия и кальция, калия и магния, кальция и магния. [39]
 |
Растворение труднорастворимых электролитов при 20 С. [40] |
Растворение труднорастворимой соли всегда сопровождается конверсией ее в другую, растворимую соль. Навстречу им из секции 2 через анионитовую мембрану к аноду мигрируют нитратные ионы. В результате в секции 3 образуются растворы нитратов катионов труднорастворимых солей. Растворение электродиализом сопровождается также концентрированием раствора, так как концентрация ионов труднорастворимой соли ограничена ее растворимостью, а в секции 3 может образовываться нитрат любой концентрации в зависимости от времени растворения и приложенного потенциала, если к тому же последний не меньше равновесного. [41]
В 1 М HNO3 скорость реакции увеличивается примерно в три раза на каждые 10 повышения температуры. При высоких концентрациях плутония скорость окисления больше, но высокие концентрации нитратных ионов снижают скорость окисления вследствие комплексообразования. [42]
При таком содержании и наличии дополнительной к диффузии поставки нитратных ионов током ожидаемые предельные скорости окисления среды должны быть больше наблюдаемых. Это значит, что для достижения наблюдаемых предельных скоростей процесса, помимо ограниченности беспрепятственной поставки нитратных ионов к поверхности анода, должны существовать еще дополнительные причины уменьшения скорости разряда нитратных ионов. В рассматриваемых условиях существование таких причин вполне возможно. Последняя причина подтверждается тем, что предельные скорости окисления среды достигаются тогда, когда скорость этого процесса начинает превышаться скоростью растворения металла. [43]
Мы видим, что медь теряет два электрона, а азотная кислота приобретает 3 электрона, но, взяв эти числа в качестве коэффициентов, мы не сможем получить правильно составленное уравнение реакции. Следует принять во внимание, что определенная часть азотной кислоты в этой реакции не восстанавливается, а лишь поставляет нитратные ионы для образования Cu ( NO3) 2 без изменения степени окисления азота. Поэтому коэффициент при HNO3 должен учитывать оба способа превращения азотной кислоты в процессе реакции. На каждые три атома меди, которые окисляются в реакции, должны приходиться две восстанавливаемые молекулы азотной кислоты и еще шесть молекул азотной кислоты, дающие нитратные ионы. [44]
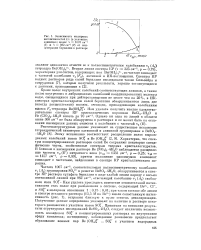 |
Зависимость молярных интенсивпостей / / с ( в условных единицах полос v 1007 см-1 ( 1 и v 982 см 1 ( 2 от концентрации бериллия в растворе. [45] |
Страницы: 1 2 3 4