Металлический галлий
Cтраница 2
Металлический галлий и безводный ОаВгз ( в количестве, несколько большем 2 моль на 1 моль металла) помещают в ампулу. Особое внимание обращают на защиту от влаги воздуха. Ампулу вакуумируют, запаивают и медленно нагревают до 180 С. Через 12 ч весь металл растворяется. [16]
Металлическим галлием пользуются, для наполнения кварцевых термометров, служащих для измерения высоких температур. Галлий плавится при 29 8 С, а закипает только при 2205 С, так что такие термометры позволяют измерять температуры до 1000 С и выше, что невозможно при употреблении обычных термометров. Добавлением галлия к алюминию получают сплавы, хорошо поддающиеся горячей обработке; сплавы галлия с золотом применяются в ювелирном и зубопротезном деле. [17]
Металлическим галлием пользуются для наполнения кварцевых термометров, служащих для измерения высоких температур. Галлий плавится при 29 8 С, а закипает только при 2205 С, так что такие термометры позволяют измерять температуры до 1000 С и выше, что невозможно при употреблении обычных термометров. Добавлением галлия к алюминию получают сплавы, хорошо поддающиеся горячей обработке; сплавы галлия с золотом применяются в ювелирном и зубопротезном деле. [18]
Металлическим галлием пользуются для наполнения кварцевых термометров, служащих для измерения высоких температур. Галлий плавится при 29 8 С, а закипает только при 2205 С, так что такие термометры позволяют измерять температуры до 1000 С и зыше, что невозможно при употреблении обычных термометров. Добавлением галлия к алюминию получают сплавы, хорошо поддающиеся горячей обработке; сплавы галлия с золотом применяются в ювелирном и зубопротезном деле. [19]
Металлическим галлием пользуются для наполнения кварцевых термометров, служащих для измерения высоких температур. Галлий плавится при 29 8 С, а закипает только при 2205 С, так что такие термометры позволяют измерять температуры до 1000 С и выше, что невозможно при употреблении обычных термометров. Добавлением галлия к алюминию получают сплавы, хорошо поддающиеся горячей обработке; сплавы галлия с золотом применяются в ювелирном и зубопротезном деле. [20]
Металлическим галлием пользуются для наполнения кварцевых термометров, служащих для измерения высоких температур. Галлий плавится при 29 8 С, а закипает только при 2205 С, так что такие термометры позволяют измерять температуры до 1000 С и выше, что невозможно при употреблении обычных термометров. Добавлением галлия к алюминию получают сплавы, хорошо поддающиеся горячей - обработке; сплавы галлия с золотом применяются в ювелирном и-зубопротезном деле. [21]
Металлическим галлием пользуются для наполнения кварцевых термометров, служащих для измерения высоких температур. Галлий плавится при 29 8 С, а закипает только при 2205 С, так что такие термометры позволяют измерять температуры до 1000 С и выше, что невозможно при употреблении обычных термометров. Добавлением галлия к алюминию получают сплавы, хорошо поддающиеся горячей обработке; сплавы галлия с золотом применяются в ювелирном и зубопротезном деле. [22]
Почему металлический галлий проявляет более слабые восстановительные свойства, чем алюминий. [23]
Действие жидкого металлического галлия на различные материалы характеризуется следующими данными. [24]
Дейтронами облучают металлический галлий. Мишень растворяют в НВг. Образовавшийся бромистый галлий отгоняют вместе с НВг. К раствору добавляют HNO3 и упаривают его досуха, после чего остаток растворяют в воде. [25]
При взаимодействии металлического галлия или индия с ал-килбромидами и - иодидами образуются главным образом соответствующие сесквигалогеннды. [26]
Выделенный описанным способом металлический галлий имеет чистоту около 99 %, основной примесью является цинк. В случае необходимости галлий подвергается дальнейшей очистке для получения особо чистого металла, используемого в электронике. [27]
После того как металлический галлий исчезнет, прибор охлаждают, отсоединяют источник хлористого водорода и впускают азот для вытеснения хлористого водорода. Возогнанный продукт извлекают из прибора и анализируют на содержание хлора и галлия обычными весовыми методами; хлор определяют в виде хлорида серебра, а галлий - в виде окиси. [28]
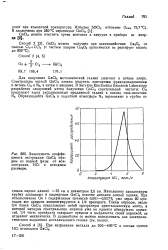 |
Зависимость коэффициента экстракции GaCl3 эфиром из водной фазы от концентрации НС1 в исходном растворе. [29] |
Для получения GaCl3 металлический галлий сжигают в потоке хлора. Спектрально чистый GaCl3 можно получить повторным фракционированием в потоке С12 и N2, а затем в вакууме. [30]
Страницы: 1 2 3 4